

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء التناسقية

الكيمياء الاشعاعية والنووية
الأحماض الامينية Amino Acids
المؤلف:
أ.د.عيسى عبد السعداوي
المصدر:
الكيمياء الحيوية النظري
الجزء والصفحة:
ص140
29-2-2016
9428
الأحماض الامينية Amino Acids
كما أسلفنا فإن الأحماض الامينية تعتبر الوحدات البنائية الاساسية، التي تشكل التراكيب الكيميائية المختلفة للجزيئات البروتينية. الأحماض الامينية مركبات عضوية بسيطة تتألف من مجموعة الامين ومجموعة الكاربوكسيل وذرة تسمى بذرة الكربون ألفا (a). وقد سميت هذه الأنواع من المركبات العضوية نسبة الى ذرة الكربون هذه بالأحماض الامينية – ألفا (a – Amino Acids). وغالبا ما تسمى مجموعة (R) في هذه الاحماض بالسلسلة الجانبية للحامض الاميني، واعتمادا على ما تتخذه هذه المجموعة (R) من تراكيب كيميائية مختلفة، اختلفت على ضوء ذلك الاحماض الامينية عن بعضها البعض. وفي ادناه الصيغة الكيميائية العامة للأحماض الامينية :
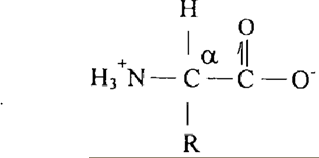
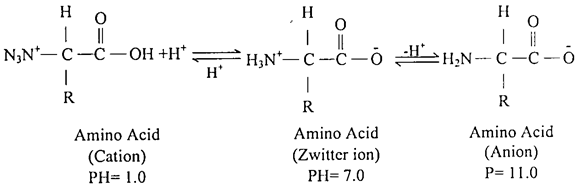
تشكل الأحماض الامينية في المحاليل المتعادلة مركبات ثنائية القطب تسمى – زويتر أيون (Zwitter Ions) بدلاً من وجودها على هيئة جزيئات غير متأينة، ففي الشكل ثنائي القطب للأحماض الامينية تفقد مجموعة الكربوكسيل بروتوناً لصالح المجموعة الأمينية التي تتحول نتيجة لذلك الى ايون موجب ومجموعة الكربوكسيل الى ايون سالب، وكما هو موضح في التركيب العام للأحماض الامينية في أعلاه. كما ان الحالة الايونية للأحماض الأمينية تختلف تبعاً لاختلاف درجة حموضة المحيط الذي يتواجد فيه الحامض الاميني. ففي المحلول الحامضي (PH = 1.0) تكون المجموعة الكربوكيسلية غير متأينة، بينما تتأين المجموعة الأمينية، اما في المحيط القاعدي (PH = 11.0) فتتأين المجموعة الكربوكيسلية وتبقى مجموعة الأمين في الحالة غير المتأينة، وكما هو موضح في التراكيب التالية :
 الاكثر قراءة في الاحماض الامينية والبروتينات
الاكثر قراءة في الاحماض الامينية والبروتينات
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة
قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)


















