

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء التناسقية

الكيمياء الاشعاعية والنووية
Cyclohexadienone Reactions Cross-Conjugated Derivatives
المؤلف:
William Reusch
المصدر:
Virtual Textbook of Organic Chemistry
الجزء والصفحة:
............
2-9-2018
2057
Cyclohexadienone Reactions
Cross-Conjugated Derivatives
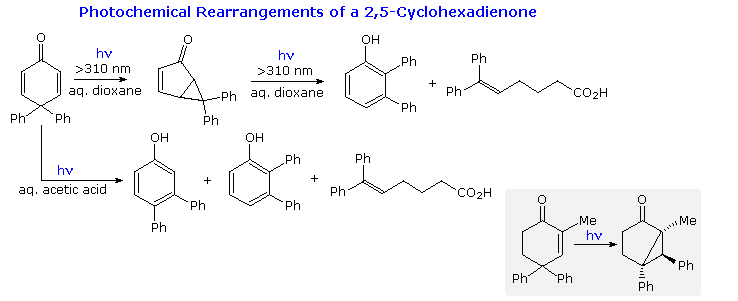
Derivatives of 2,5-cyclohexadienone are common in nature, and their photochemical transformations posed a challenge to early researchers. Some reactions of 4,4-diphenyl-2,5-cyclohexadienone are presented in the following diagram. Although 2,3-diphenylphenol was a product from irradiation in aqueous dioxane, it is actually formed from 6,6-diphenylbicyclo[3.1.0]hex-3-ene-2-one, the initial rearrangement product. It should be noted that a similar bicyclo[3.1.0]hexane isomer was formed by irradiation of 4,4-diphenyl-2-cyclohexenones, as shown in the gray-shaded box at the bottom right.
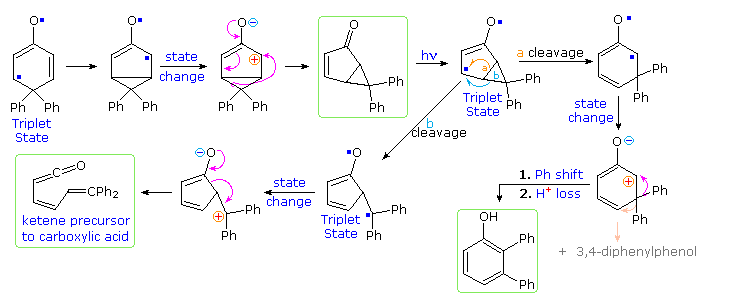
These photochemical rearrangements occur by way of triplet excited states, which are conveniently depicted as diradicals. Mechanisms for these reactions will be displayed above . Bond reorganization may take place in the triplets, which eventually intersystem cross to singlet species. Charge separation in these states may then lead to rearrangement to a stable product.
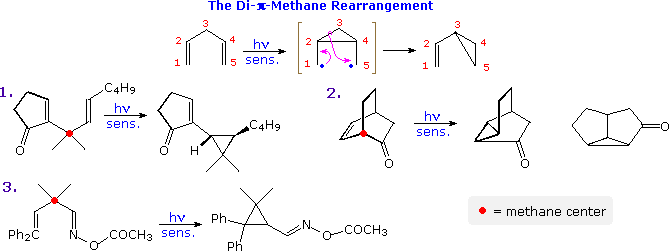
The photo-isomerization shown above is one example of a general family of reactions known as di-π-methane rearrangements, other examples of which are illustrated in the following diagram. These transformations are often photo-sensitized, indicating they proceed by way of triplet excited states. As the name suggests, substrates exhibiting this rearrangement are comprised of two π-functions separated by a saturated (sp3-hybrid) carbon atom (designated by a red dot in the illustration). In the event, a 1,2-shift of one ene-group, followed by a bond formation between the terminal sites of the remaining π-function leads to a vinylcyclopropane product. One of the unsaturated functions may be a carbonyl or imine group, as in examples 2. and 3.
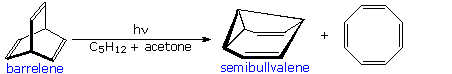
A photo-isomerization of this kind was used by H. Zimmerman (Wisconsin) to prepare the novel self-replicating diene semibullvalene from barrelene.
 الاكثر قراءة في تجارب وتفاعلات في الكيمياء العضوية
الاكثر قراءة في تجارب وتفاعلات في الكيمياء العضوية
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة
قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)


















