


 الفاكهة والاشجار المثمرة
الفاكهة والاشجار المثمرة
 نخيل التمر
نخيل التمر
 الحمضيات
الحمضيات 
 الاشجار ذات النواة الحجرية
الاشجار ذات النواة الحجرية
 المحاصيل
المحاصيل
 المحاصيل البقولية
المحاصيل البقولية
 محاصيل الالياف
محاصيل الالياف
 محاصيل زيتية
محاصيل زيتية
 محاصيل الحبوب
محاصيل الحبوب 
 محاصيل الخضر
محاصيل الخضر
 القرعيات
القرعيات 
 المحاصيل المنبهة و المحاصيل المخدرة
المحاصيل المنبهة و المحاصيل المخدرة
 المحاصيل السكرية
المحاصيل السكرية 
 نباتات الزينة والنباتات الطبية والعطرية
نباتات الزينة والنباتات الطبية والعطرية
 الحشرات النافعة
الحشرات النافعة
 النحل
النحل 
 دودة القز(الحرير)
دودة القز(الحرير)
 تقنيات زراعية
تقنيات زراعية
 التصنيع الزراعي
التصنيع الزراعي 
 الانتاج الحيواني
الانتاج الحيواني 
 الطيور الداجنة
الطيور الداجنة
 الاسماك
الاسماك
 الابقار والجاموس
الابقار والجاموس
 الاغنام
الاغنام 
 آفات وامراض النبات وطرق مكافحتها
آفات وامراض النبات وطرق مكافحتها 
 الحشرات
الحشرات 
 امراض النبات ومسبباتها
امراض النبات ومسبباتها 
 الحشائش والنباتات الضارة
الحشائش والنباتات الضارة |
أقرأ أيضاً
التاريخ: 29-6-2018
التاريخ: 2-7-2018
التاريخ: 29-6-2018
التاريخ: 29-8-2017
|
مراحل الإصابة الفايروسية
إن الفايروس الناجح هو الذي يتمكن من التضاعف في خلايا النبات المصاب بعد دخوله فيها ثم الحركة من الخلايا المصابة إلى بقية أنسجة النبات لذا فان نجاح الإصابة الفايروسية الجهازية يتطلب تضاعف الفايروس أولا داخل الخلايا المصابة ثم حركته من الخلية المصابة إلى الخلايا المجاورة السليمة وتكرار الإصابة والحركة وصولا إلى الأوعية الناقلة، عليه تمر الإصابة الفايروسية بالمراحل المتتالية التالية في النبات العائل.
1. مرحلة وصول ودخول الفايروس إلى النبات
تصل الفايروسات إلى النباتات بوسائل النقل المختلفة وتلعب الناقلات بأنواعها الدور الأهم في نقل عدد كبير من أنواع الفايروسات وإيصالها إلى النباتات السليمة ثم تلقيحها بالفايروس وإدخاله إلى خلاياها حيث تخترق السطح النباتي المكون من الشمع والكيوتكل والجدر الخلوية التي لا تستطيع الفايروسات اختراقها، لذا ولتحقيق الإصابة فإنه يجب أن تدخل الفايروسات إلى النباتات ميكانيكيا عبر خلايا البشرة المجروحة بجروح غير مميتة Sub lethal wounds أي المزال عنها جدارها الخلوي ويتحقق ذلك حينما تصل الجسيمات الفايروسية محمولة بعصير النبات المصاب وتدخل في الخلايا المجروحة أو تدخل مباشرة بواسطة الناقلات بأنواعها والتي تخرق الطبقات النباتية أعلاه وتنقل الفايروسات أثناء تغذيتها، ولم يسجل دخول أي فايروس نباتي عن طريق الفتحات الطبيعية في النبات وهي الثغور والعديسات والثغور المائية والغدد الرحيقية.
2. تضاعف فايروسات النبات
تأخر فهم آلية تضاعف الفايروسات النباتية في عوائلها مقارنة بالمعلومات المتوفرة عن تضاعف الفايروسات البكتيرية أو البشرية أو غيرها من الفايروسات وذلك بسبب تأخر تطوير تقانات زراعة الأنسجة النباتية في أوساط زرعيه صناعية لغاية سبعينات القرن العشرين وهي التقانات التي تتيح دراسة تضاعف الفايروسات وتصرفها في الخلايا في أنسجة معزولة خارج جسم النبات مما يسهل العمل وسرعة الحصول على النتائج حيث طورت تقانات تخليق البروتين في خلايا مفصولة حرة خارج النسيج النباتي الحي وزراعة البروتوبلاست وزراعة خلايا الناقلات الحشرية للفايروسات في بيئات زرعيه خاصة وكذلك تقانات تضاعف الفايروسات خارج النبات الحي باستعمال رايبوسومات أجنة الحنطة Wheatgram System أو في بكتريا القولون Escherichia coli أو في خلايا دم الأرانب Rabbit reticulocyte system او تسمى Rabbit anaemic blood cells ان الزراعة النسيجية للبروتوبلاستات Protoplasts وهي خلايا نباتية تم فصلها عن النسيج النباتي وإزالة جدارها الخلوي الصلب بإنزيمات السليليز والبكتينيز ثم زراعتها في أوساط زرعية خاصة قد سهل كثيرا دراسة تضاعف الفايروسات وذلك لأن هذه التقانة ألغت مشكلة عقبة الجدار الخلوي الذي يستحيل اختراقه من قبل الفايروسات حيث اعتمدت التجارب التي كان يجريها الباحثون قبل ابتكار هذه التقانة على تلقيح خلايا النبات ميكانيكيا بالفايروس بالطريقة التقليدية وهي التي تتطلب نظريا جرح 10000 خلية نباتية لكي تصاب خلية واحدة يتحقق فيها شرط الجرح غير المميت، كذلك فان كل خلية ملقحة تتطلب 100 ألف جسيمة فايروسية لتحقيق الإصابة ولكن عند استعمال زراعة البروتوبلاست فان 50% من البروتوبلاست الملقحة ستصاب بالفايروس ولا يحتاج كل برتوبلاست لأكثر من 10-100 جسيمة لكي يصاب كما أن تركيز الفايروسات يكون عاليا فيه إذ وصل تركيز فايروس موزائيك التبغ (TMV) إلى ما يقرب من 610 جسيمة/بروتوبلاست بعد التحضين لمدة 24 ساعة عند 25م.
يعتمد تضاعف الفايروسات على جينوماتها التي تتباين في أنواعها حسب نوع الفايروس، ويبين الجدول (1) أنواع جينومات فايروسات النبات حسب نوع الجينوم وعدد قطعه مع الأجناس الفايروسية الممثلة لكل نوع حيث تتباين آليات تضاعف الفايروسات حسب أنواع جينوماتها، إلا أنها تشترك باليات عامة فهي جميعا تبدأ بالتضاعف مباشرة بعد دخولها إلى سايتوبلازم خلايا النبات العائل، وفيما يأتي خطوات تضاعف الفايروس النباتي.
2.1. مرحلة نزع الغطاء البروتيني (ازالة الكابسيد)
تشترك كل الفايروسات وبغض النظر عن نوع جينومها في خطوة نزع الغطاء البروتيني Uncoating or Decapsidation حيث تدخل كل أنواع الفايروسات إلى النباتات بشكل فايروس كامل (الفريون) Virion أو يسمى Intact Virus أي الجسيمة الفايروسية بكل مكوناتها. يبدأ تفكيك الغطاء البروتيني إلى وحداته البنائية البروتينية الأساسية Protein Subunits لتحرير الجينوم كي يتمكن من إظهار (ترجمة) معلوماته الوراثية أي تفعيل جيناته ويحصل ذلك خلال ساعات من دخول الفايروس إلى الخلية ويرجح تفكيك أغطية الفايروسات بسيطة التركيب المكونة من الحامض النووي والكابسيد خلال الفترة النشطة بايوكيميائيا من دورة حياة الفايروس، فيما تتفكك اغلفة الفايروسات المعقدة ومنها فايروسي الاصفرار التماوتي للخس (LNYV) والتورم الجرحي (WTV) جزئيا خلال هذه الفترة ولكنها تبقى محتفظة بجزء قليل من البروتين المكون لجوهر الجسيمة (اللب) Core.
الجدول (1): انواع جينومات فايروسات النبات
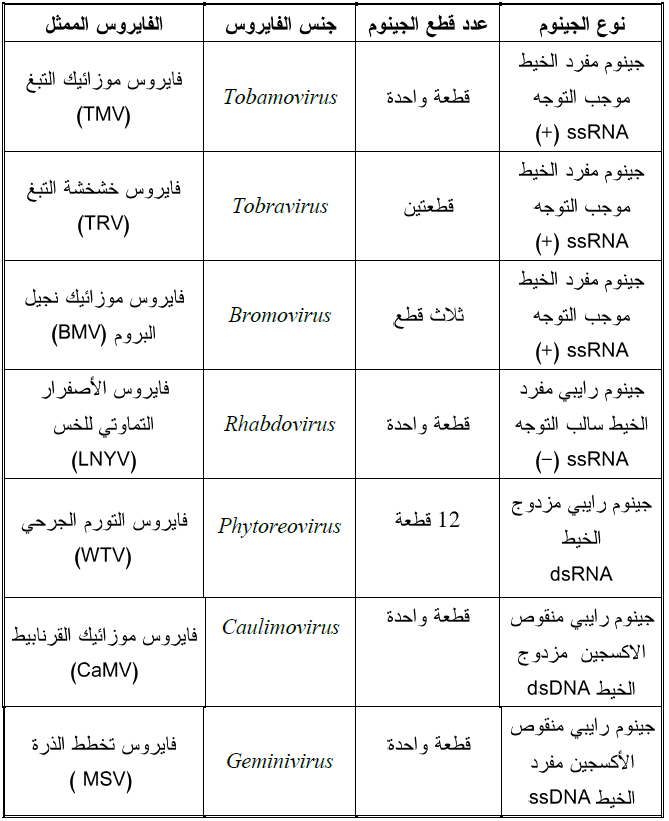
توجد علاقة بين نزع الغطاء والمدى العائلي للفايروسات إذ وجد عند تغليف جينوم فايروس موزائيك نجيل البروم (BMV) بالغطاء البروتيني لفايروس موزائيك التبغ فانه يصبح غير معدي لنباتات الشعير وهو العائل الأساسي لذلك الفايروس، كذلك تتأثر عملية نزع الغطاء بأي استبدال لحامض أميني بأخر يدخل في بناء الغطاء. من الأدلة المهمة التجريبية على نزع الغطاء البروتيني للفايروسات مباشرة بعد دخولها خلايا العائل هي أن تلقيح نباتات التبغ بالجينومات العارية لفايروس موزائيك التبغ أدى إلى ظهور الإصابة بوقت أسرع مقارنة بتلقيحها بالجسيمات الكاملة كذلك حصول ظاهرة التنشيط الضوئي لجينومات الفايروسات Photoreactivation بعد تعريضها للأشعة السينية أو الأشعة فوق البنفسجية وهذا دليل على عدم وجود الغطاء البروتيني لأن وجوده يمنع حدوثها ووجد أيضا أن 25% من كمية البروتين في فايروس موزائيك التبغ قد ترسبت بعد ثمانية دقائق فقط من تلقيح نباتات التبغ به. تتباين آليات تفكيك الأغطية البروتينية لفايروسات النبات حسب تركيب الفايروسات وكما يلي:
أ- تفكيك الفايروسات العصوية
تبدأ الإصابة الفايروسية بإزالة الكابسيد عن الجينوم بما يكفي لترجمة أول هيكل تشفيري مفتوح Open Read Frame , ORF ووجد أن أيون الكالسيوم Ca++ يبطئ أو يعيق تفكيك وحدات الكابسيد عند الأس الهيدروجيني 9 ويدل ذلك أن مواقع ارتباط أيون الكالسيوم في الخلية Ca++ binding sites تعمل مفتاح سيطرة لعملية التفكيك وأن إزالة أيون الكالسيوم يحدث تغييرا في بنية الوحدات البروتينية مما يؤدي إلى تفككها، ويعتقد أن الفايروسات بسيطة التركيب ومنها فايروس موزائيك التبغ تتفكك أغطيتها عند الغشاء الخلوي لخلية العائل أو في داخله حيث يكون تركيز أيون الكالسيوم مرتفعا وهو 10-3 مولر في الوقت الذي يكون تركيزه داخل الخلية 10-7 مولر وبالتالي يوفر هذا التركيز الأيوني في الأغشية طاقة تكفي لتفكيك الأواصر البينية للوحدات البروتينية ولكن لا زالت هذه الفرضية مثار جدل.
ولقد أجرى الباحثون العديد من التجارب المختبرية خارج النسيج الحي وباستعمال تقانات متعددة لدراسة آليات تفكيك الغطاء البروتيني وأجريت أغلب هذه الدراسات على فايروس موزائيك التبغ باستعمال جسيماته المعلمة شعاعيا Radioactively labeled particles سواء بتعليم الغطاء أو الجينوم حيث تم تفكيك البروتينات باستعمال القلويات Alkaloids أو المنظفات Detergents ومنها مركب "كبريتات دوديسيل الصوديوم" تركيز Sodium dodecyl sulphate, SDS%1 الشائع الاستعمال في هذا المجال حيث تقوم هذه المركبات بنزع الوحدات البروتينية لجينوم فايروس موزائيك التبغ وتبدأ عملية التفكيك من النهاية 5 للجينوم وهي النهاية المقعرة Concaved end للجسيمة الفايروسية ويؤدي هذا التفكيك إلى إنتاج سلسلة من الجسيمات الفايروسية دون الحجم الحقيقي للفايروس Subvira rods وبأطوال متباينة، وأدى وضع جسيمات فايروس موزائيك التبغ لفترة قصيرة في وسط محلول الرنا المراسل باستعمال معلق الخلايا الدموية للأرانب ذو الأس هيدروجيني بقيمة 8 إلى إنتاج أنواع من عديد الببتيد الفايروسي ويفسر ذلك ان الوسط القاعدي يؤدي إلى إزالة ثباتية الكابسيد Destabilize عند النهاية 5 للجينوم بما يكفي لرايبوسومات الخلية للارتباط مع التعاقب الجينومي الريادي leader Sequence 5 ثم تتحرك نزولا على طول الجينوم مستبدلة الوحدات البروتينية للغطاء وهذا يعني أن الرايبوسومات الخلوية هي المسئولة عن عملية تفكيك الغطاء البروتيني الفايروسي بواسطة الية معقدة تسمى "التفكيك الترجمي المرافق" Co-transitional disassembly واطلق مصطلح "الستربتوسومات" Sriptosomes علي الرايبوسومات التي تقوم بالتفكيك، وأطلق على حالة ارتباط الرايبوسومات مع الكابسيد مصطلح " المعقد الرايبوسومي المزيل الجزئي للغطاء " Ribosome partially Stripped rod Complex، (الشكل 1) وأجريت تجارب مماثلة باستعمال أجنة القمح وعند الأس الهيدروجيني 8 فأنتجت الجسيمات الفايروسية كمية من عديد الببتيد تزيد بثلاثة أضعاف عن كميته المنتجة من قبل الجينوم الموجود في خلايا النبات المصاب وهذا يشير إلى قدرة فايروس موزائيك التبغ ومن خلال هذه الألية على حماية حامضه النووي داخل العصية من الإنزيمات المحللة للأحماض النووية خلال مرحلة نزع الغطاء الحرجة بسبب ما ينتجه من عديد الببتيد الذي يعيد تغليف الجينوم، وتوفرت أدلة أخرى دعمت هذه الآلية من تجارب تخليق البروتينات خارج النسيج الحي باستعمال بكتريا القولون وعند أس هيدروجيني 8 حيث أعطى الجينوم المخلق في البكتريا كمية كبيرة من البروتين ذو الحجم 126 كيلودالتون فيما أعطى الجينوم العادي المخلّق في خلايا النبات المصاب بروتينا بحجم 50 كيلو دالتون أو أقل مع كميات من بروتين الغطاء، ووجد أنه عند معاملة جسيمات فايروس موزائيك التبغ بمادة SDS لمدة 15 ثانية فقد أدى ذلك إلى تعرية تعاقبا نيوكليوتايديا من الطرف 5 وإلى ما وراء الكودون AUG ولكن لم يتم تجاوز حدود هذا التعاقب كما لم يتم تعرية التعاقبات التالية خلال الخمسة عشرة دقيقة التالية من التعريض لتلك المادة، ووجد أنه عند تحضين الجسيمات الفايروسية مع خلاصة أجنة القمح أو خلايا دم الأرانب أدى ذلك إلى ارتباط رايبوسوما واحدا أو أثنين مع حوالي 20% من الجسيمات الفايروسية.
واستعمل البروتوبلاست في دراسة تجارب نزع الغطاء باستعمال القلويات الضعيفة ومادة SDS حيث لقحت برتوبلاستات بشرة نبات التبغ المصاب بفايروس موزائيك التبغ وأضيفت جزيئات الرايبوسوم 80S التي تحركت على طول الجينوم من النهاية 5 حيث أمكن عزل معقدات بروتينية مماثلة لخواص الستربتوسومات وذلك بعد فترة من تلقيح البرتوبلاستات، ووجد أن الرايبوسوم يرتبط بالجينوم بعد إرخاء الفريون مما يؤدي إلى كشف جزء من النهاية 5 فيصبح الجينوم في متناول الرايبوسوم حيث أن التعاقب الريادي الذي بحجم 68 نيوكليوتايدة والذي تنقصه قاعدة الكوانين يرتبط بشكل ضعيف جدا مع وحدات الغطاء البروتيني مقارنة ببقية مناطق الجينوم وكانه مهياً أصلا للتفكك ويفسر ذلك بان الوحدات البروتينية لهذا الفايروس ترتبط مع بعضها بأواصر كاربوكسيلية حيث تتكون أصرتين كاربوكسيليتين بين كل وحدتين متجاورتين مع وجود آصرة كاربوكسيلية آخري بين كل وحدة بروتينية والجينوم وتصبح هذه الأواصر في الوسط الضعيف قاعديا موجبة الشحنة بروتونية مما يؤدي لحدوث تنافر كهربائي مستقر Electrostatic repulsion وبذلك تتفكك اغطية الفايروسات قبل أن يعمل عليها الرايبوسوم لتبدأ عملية التفكيك الترجمي المرافق بارتباط الرايبوسوم بالجينوم ويبدأ بترجمة الهيكل التشفيري المفتوح الأول لفايروس موزائيك التبغ وهو 5-ORF1 فيخلق أنزيم الربلكيز بحجم 128/126 كيلودالتون مستبدلا الوحدات البروتينية للغطاء، وعندما يصل الرايبوسوم إلى "الكودون الموقف" Stop Codon وهو الهيكل التشفيري المفتوحORF 128/126 فان الرايبوسوم ينفصل عن الجينوم، وأثيرت التساؤلات حول كيفية تفكيك الربع الأخير من الجسيمة الفايروسية وتحديدا في النهاية 3 إذ لا يصل الرايبوسوم إلى هذا الجزء بل يبدأ عمله من النهاية 5 لذلك يعتقد أن إنزيم الربلكيز هو الذي ينجز المهمة بدلا عن الرايبوسومات بتحركه على الجينوم بالاتجاه 3-5 وتخليقه للخيط التضاعفي الوسيط السالب Strand replication intermediate (-) خلال عملية التضاعف ويعني ذلك أن تفكيك الغطاء البروتيني لفايروس موزائيك التبغ يحصل بطريقة ثنائية الاتجاه وفق آلية "التفكيك التضاعفي المرافق" لذلك يطلق عليه "التفكيك ثنائي الاتجاه" - Bi directional disassembly وهو مصطلح مرادف لمصطلح "التفكيك الترجمي المرافق" وهي الألية التي تعمل على الجينوم بالاتجاه 3-5 لإنتاج إنزيم الربلكيز الذي يكمل عملية التفكيك لما تبقى من الجسيمة بالاتجاه 3–5، (الشكل 2) وهذا دليل على أن عمليتي التضاعف والتفكيك هما عمليتين متزامنتين مترافقتين Coupled processes وهي عملية سريعة تفكك الغطاء البروتيني خلال 20 دقيقة، كما وجد أن كل جسيمة فايروسية تعمل عليها اربعه رايبوسومات في وقت واحد لتفكيكها.
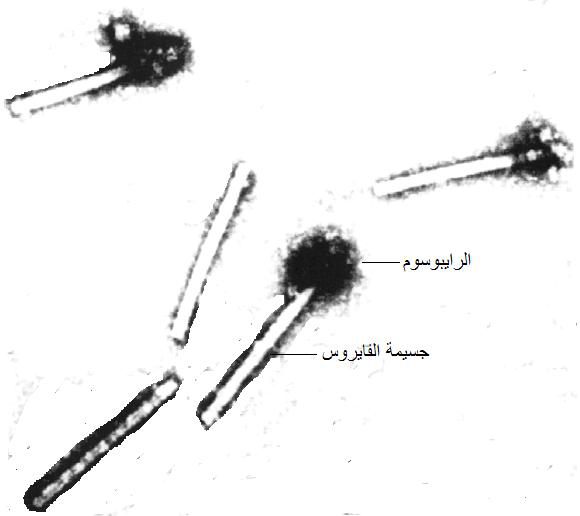
الشكل (1): صورة بالمجهر الالكتروني لمعقدات الرايبوسومات - الفايروسات والمسماة "الستربتوسومات" Striptosome complexes التي تلعب دورا محتملا في عملية التفكيك الترجمي المرافق Co-translational disassembly process والتي تكونت من خلال تفاعلات الترجمة لفايروس موزائيك التبغ (TMV) خارج النسيج الحي، ويلاحظ ارتباط إحدى نهايات بعض الجسيمات بتراكيب يعتقد آنها رايبوسومات.
الشكل مقتبس من Hull 2002.
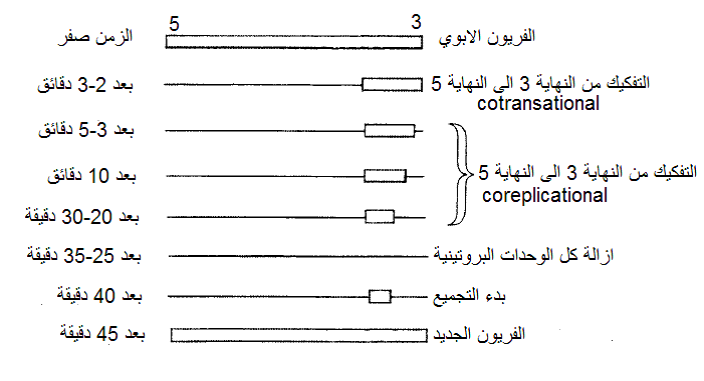
الشكل (2): التفكيك ثنائي الاتجاه Bidirectional disassembly لفايروس موزائيك التبغ (TMV) داخل بروتوبلاست خلية العائل حيث تزال الوحدات البروتينية للغطاء بالاتجاه 5-3 أولا من حوالي 75% منه وذلك في أول 2-3 دقائق بعد تلقيح البروتوبلاست بالفايروس، أما إزالة الغطاء من النهاية 3 فتبدأ بعد وقت قصير من بدايتها من النهاية 5، لتكتمل إزالة الوحدات البروتينية بالاتجاه 3-5 بعد حوالي 25-35 دقيقة، ثم يبتدئ إنشاء الغطاء البروتيني أي تجميع Assembly الخيط الرايبي الجديد بعد حوالي 30-40 دقيقة من الإصابة ويكتمل عند الدقيقة 45.
الشكل مقتبس منHull 2002.
ب- تفكيك الفايروسات البلورية
أجريت أغلب هذه الدراسات على فايروسات Bromoviruses وخاصة فايروسي موزائيك نجيل البروم (BMV) وفايروس التبرقش الأصفر للوبيا (CCMV) وباستعمال أجنة الحنطة كوسط للتضاعف والتي أظهرت حصول انتفاخ الجسيمات الفايروس الأول في وسط يزيد فيه الأس الهيدروجيني عن 7 ويسمح هذا الانتفاخ بحصول آلية التفكيك الترجمي المرافق كما في الفايروسات العصوية وبذلك يعد الانتفاخ ضروريا كمرحلة تسبق مباشرة تفكيك أغطية هذه الفايروسات، ووجد أن الأيون الكالسيوم دورا فيها ولكن أظهر الفايروس الثاني أدلة تشكك في هذه الألية حيث لم تنتفخ جسيماته تحت الظروف القلوية لذا اقترحت الية بديلة وهي حصول تحول تركيبي في الأغطية بتأثير الأس الهيدروجيني يؤدي إلى تفككها وبذلك يصبح الجينوم في متناول النظام الترجمي وهذه الألية مماثلة لتلك الملاحظة مع الفايروسات الحشرية والفقارية وتفترض بأن النهاية النتروجينية المكونة من خمس وحدات بروتينية والموجودة في الكابسومير الخماسي لكابسيد تخضع التحول تركيبي كبير يبتدئ من داخل الفريون الي خارجه مما يسمح بتكوين قناة يعبر من خلالها الجينوم ليصبح في متناول النظام الترجمي إلا أن هذا يتطلب تحرير النهاية 5 أيضا وهذا يعني أنها مرتبطة مع الكابسومير الخماسي.
2.2. مرحلة تضاعف الحامض النووي الفايروسي
يبدأ الحامض النووي الفايروسي (الجينوم) بالتضاعف فور انتهاء عملية تفكيك الغطاء البروتيني ولكن تتباين آليات التضاعف حسب نوع الحامض النووي الفايروسي وفردية أو ازدواج خيطيه وهل هو سالب أو موجب التوجه، وتتماثل آليات تضاعف جينومات فايروسات النبات عموما مع آليات تضاعف واستنساخ الأحماض النووية الخلوية وفهمت آليات تضاعف العديد من أنواع فايروسات النبات باقتباس اليات تضاعف الفايروسات الحيوانية والبكتيرية كما ساعد تطور علم الحياة الجزيئي Molecular Biology في ذلك خصوصا أن بعض الفايروسات أصبحت أداة هامة لنقل الجينات في تقانات الهندسة الوراثية.
يبدأ الجينوم الفايروسي بالتضاعف وبغض النظر عن نوعه مباشرة بعد نزع الغطاء البروتيني وتحرير الجينوم فإذا كان الجينوم من النوع الرايبي مفرد الخيط موجب التوجه Sense SSRNA(+) فان الجينوم بكامله يسلك سلوك الرنا المراسل mRNA، أما الأنواع الأخرى من الفايروسات فإنها لا تسلك سلوك الرنا المراسل ولكنها تخلق عدة نسخ من الرنا المراسل الفايروسي Viral mRNA والتي تقوم بتشفير نواتج جينية بروتينية أهمها إنزيم الربلكيز الفايروسي Viral replicase فضلا عن بروتينات أخرى تشارك في التضاعف لإنتاج أنواع من الجينومات الرايبية الثانوية Subgenomic RNAS وكذلك لتخليق جينومات فايروسية جديدة، ويتم لاحقا إنتاج بروتينات الغطاء وبروتين الحركة المسئول عن نقل الجسيمات الفايروسية من خلية لأخرى وأيضا بروتين النقل بالناقل إن كان الفايروس منقول بناقل وتنتج هذه البروتينات في مرحلة متأخرة من دورة التضاعف الفايروسي، وتشفر عدد من الفايروسات ومنها الأنواع التابعة للجنس Comovirus بروتينا بحجم كبير يسمى Polyprotein or Long polyprotein، (الشكل 3) والجدول (2). إن المعلومات الوراثية اللازمة لتشفير الغطاء البروتيني لا تأخذ إلا جزءا بسيطا من حجم الجينوم، ولغرض إنتاج غطاء بروتيني بحجم 200 حامض أميني فان الفايروس يحتاج إلى جينوم ذو وزن جزيئي 200 كيلودالتون أي قطعة جينومية بوزن كيلودالتون واحد لكل حامض أميني وهذا لا يشكل أكثر من 10% من حجم جينوم رايبي بوزن 2x10 6 دالتون أما المتبقي من حجم الجينوم فهو لتشفير إنزيم التضاعف والبروتينات الأخرى ومنها بروتين الحركة والنقل بالناقل. يتم تجميع الجينومات الفايروسية مع الوحدات البروتينية للغطاء لتكوين الفريونات في سايتوبلازم خلايا العائل عادة ثم تتحرك إلى الخلايا المجاورة لإحداث الإصابة الجهازية.
تتلخص آليات التضاعف التي ذكرت أعلاه باستنساخ الجينومات الفايروسية من الرنا المراسلة الرايبية الفايروسية mRNAS والمتمثلة بجينومات الفايروسات من النوع الرايبي مفرد الخيط موجب التوجه Sense ssRNA (+) أو المتمثلة بمستنسخات Transcripts جينومات الفايروسات سالبة التوجه Sense SSRNA (-) وجينومات الفايروسات من النوع dsRNA أو dsDNA، يبين الشكل (4) مسارات استنساخ الجينومات الفايروسية باختلاف أنواعها. يتم تضاعف الجينوم الفايروسي من الجينوم الأبوي في أنواع الفايروسات مزدوجة الخيط سواء كانت dsRNA أو dsDNA بطريقة "التضاعف شبه المحافظ "-Semi Conservative replication حيث تنتج هذه الطريقة جينوما مماثلا للجينوم الأبوي إذ ينفصل الخيطين الأصليين للجينوم الأبوي عن بعضهما أولا ثم يكون كل منهما خيطه التكاملي وكما مبين في الشكل (5) ومن المعروف أن الدنا المزدوج في الكائنات الحية يتضاعف بثلاث طرق وهي (1) طريقة "التضاعف المحافظ" Conservative replication حيث يعود الخيطين الأصليين للجينوم بعد انفصالهما وتخليق الخيطين الجديدين إلى الارتباط ثانية فيما يرتبط الخيطين الجديدين معا (2) طريقة "التضاعف شبه المحافظ" Semi-conservative replication (3) طريقة التضاعف المشتت" Dispersive replication حيث تتوزع قطع الجينوم الأبوي عشوائيا في خيطي الجينوم الوليد.

الشكل (3): البروتينات الكبيرة Polyprotein , Long polyprotin التي تشفرها فايروسات Comoviruses والناتجة من الهيكلين التشفيرين المفتوحين الاول والثاني ORF1 , ORF2 والتي يتم شطرها لاحقا الى بروتينات وظيفية صغيرة بواسطة انزيم تحليل البروتين Protease عالي الفعالية والذي تشفره هذه الفايروسات. تشير الارقام الى حجم البروتينات بالكيلودالتون (K).
الشكل مقتبس من Cann (2005).
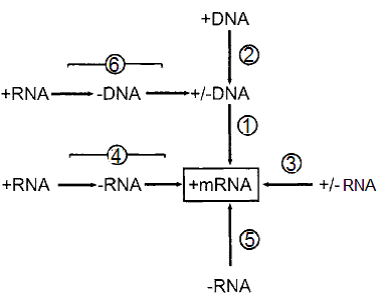
الشكل (4): مسارات اظهار الجينوم الفايروسي عن طريق الرنا المراسل Mrna.
المسار الأول: استنساخ dsDNA بواسطة "إنزيم كوثرة الرنا المعتمد على الدنا" DdRp كما في فايروسات. Caulimoviruses المسار الثاني: استنساخ ssDNA لتكوين dsDNA القالب والذي سيسلك سلوك مثيله في المسار الأول كما في فايروسات.Geminiviruses المسار الثالث: استنساخ dsRNA والذي يتم عادة بواسطة "إنزيم كوثرة الرنا المعتمد على الرنا" RdRp المشفر من قبل فايروسات Reoviruses. المسار الرابع: تضاعف الخيط الرايبي المفرد الموجب SSRNA(+) عبر الخيط السالب القالب بواسطة الإنزيم RdRp المشفر بالفايروس ويعمل الخيط الرايبي السالب قالبا للترجمة كما في أغلب فايروسات النبات ومنها فايروسات Potyviruses. المسار الخامس: استنساخ الخيط السالب الفايروسي بواسطة الإنزيم RdRp الذي تشفره فايروسات Tospoviruses. المسار السادس: الاستنساخ العكسي Reverse transcriptase للحامض الرايبي مفرد الخيط SSRNA للفايروسات العكسية وجار العكسية Retroviruses and pararetroviruse مما يؤدي إلى إنتاج قالب من dsDNA لاستنساخ الرنا المراسل mRNA.
الشكل مقتبس منHull 2002.
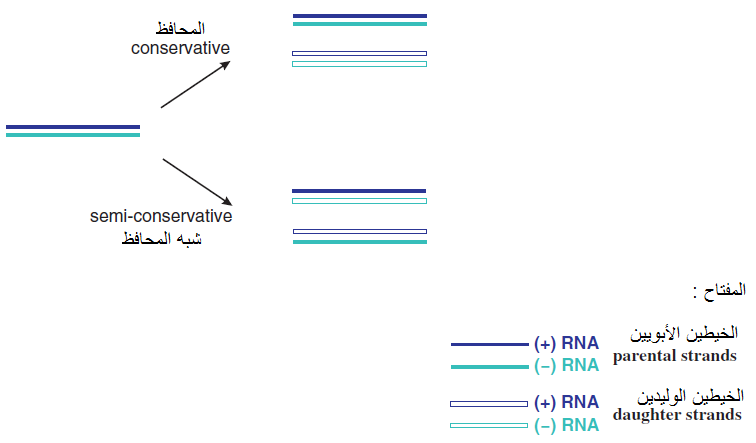
الشكل (5): طريقتي التضاعف المحافظ وشبه المحافظ للحامض النووي الرايبي مزدوج الخيط dsRNA وهي ذاتها التي تحصل مع.dsDNA
الشكل مقتبس من Mahy و Van Regenmortel 2008.
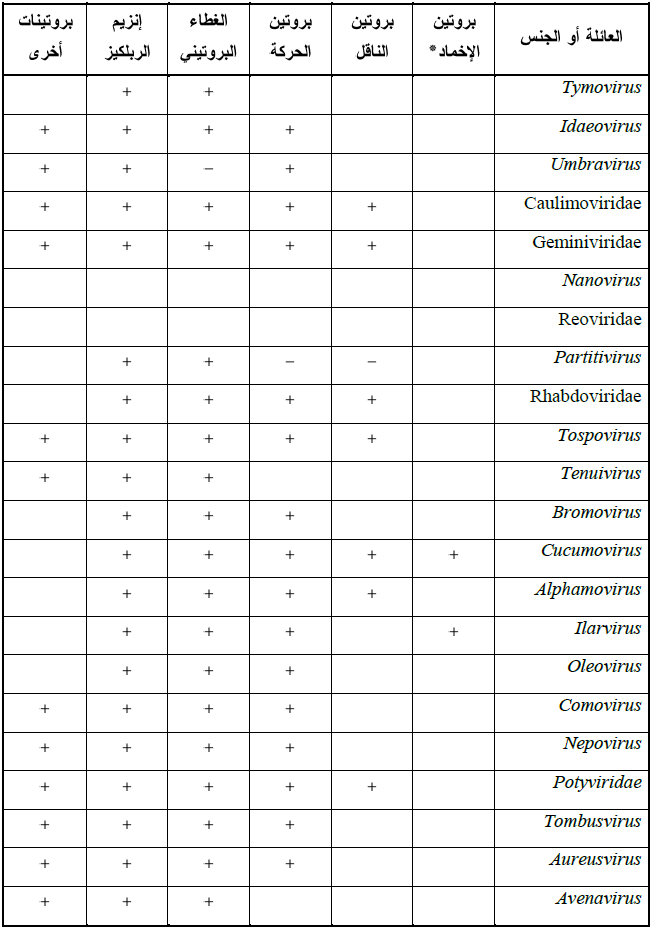
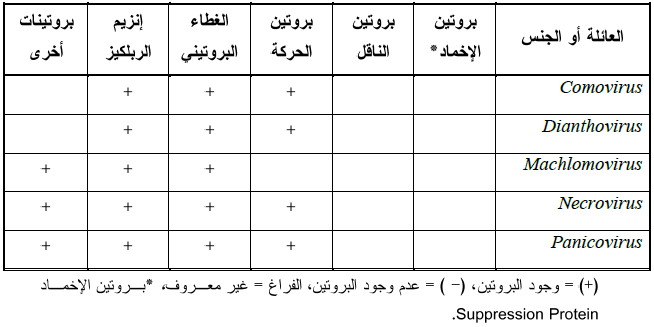
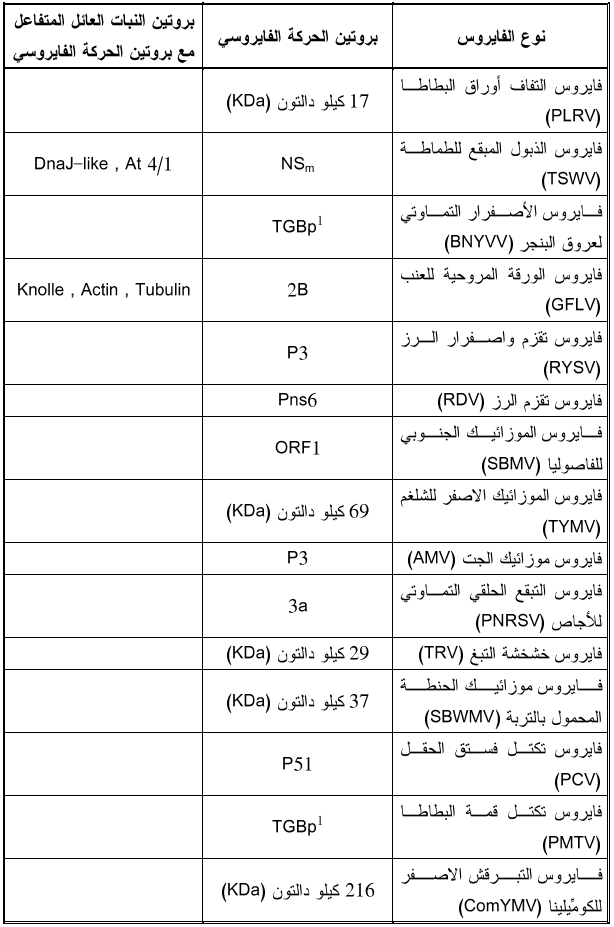
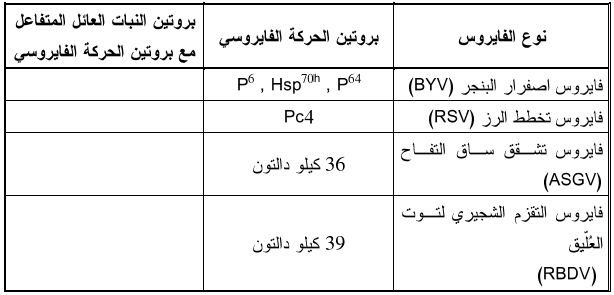
الجدول (2): البروتينات التي تشفرها اجناس فايروسات النبات

أ- تضاعف الفايروسات الرايبية مفردة الخيط موجبة التوجه sense ssRNA viruses(+)
تشكل هذه الفايروسات الغالبية العظمى من فايروسات النبات بسيطة التركيب ويطلق على جينومها بعد تفكيك الغطاء البروتيني مصطلح "الرنا الفعال" Infective RNA لقدرته المباشرة على التضاعف في خلية العائل وسلوكه سلوك الرنا المراسل الخلوي ويسمى أيضا "الخيط الموجب" Strand (+) أو "الخيط الأبوي" Parent Strand والذي يحمل عددا قليلا من الجينات الفايروسية تشفر بعضها بروتين الغطاء فيما تشفر الأخرى إنزيم التضاعف RNA Synthetase or RNA replicase والذي يتحلل بسرعة بإنزيمات تحليل الأحماض النووية الخلوية RNase الموجودة في السايتوبلازم، لذا فان تضاعف هذه الفايروسات يحصل في النواة أو مرتبطا مع المايتوكوندريا تجنبا لتأثير هذا الإنزيم. تعتمد آلية التضاعف التي تمارسها هذه الفايروسات على استعمال إنزيم بلمرة الرنا الموجه بالرنا" RNA dependent RNA polymerase (RdRp) ويطلق عليه ايضا "انزيم بلمرة الرنا" RNA polymerase القادر على تخليق الرنا من الرنا، وهو إنزيم لا تمتلكه الخلايا الحية بكل أنواعها ويعمل على الخيط الأبوي الموجب لتخليق الخيط السالب التكاملي Complementary Strand Or Antigenome (-) وذلك بعد ارتباط الإنزيم بالنهاية 3 للخيط الموجب وتحركه عليه لغاية النهاية 5 واستعماله كقالب Template وبذلك يتكون الخيط السالب الموازي والمعاكس بالاتجاه للخيط الموجب، بعدها يعود الإنزيم ليرتبط بالنهاية 3 للخيط السالب ويتحرك عليه باتجاه النهاية 5 ليخلق خيوطا جديدة موجبة وهي "الذرية" Progeny والتي تماثل الخيط الأبوي الموجب، وتستمر عملية تخليق الذرية في الخلية المصابة والتي يطلق عليها مصطلح "التضخيم" Amplification للدلالة على استنساخ الذرية الفايروسية. يطلق على الخيطين المتكاملين الموجب والسالب مصطلح "الشكل التضاعفي" Replicative Form , RF وهو عبارة عن حامض الرنا الفايروسي كامل الازدواج والذي لا يعرف دوره بدقة في عملية التضاعف الفايروسي ولكنه قد يمثل جزيئات لحامض رنا فايروسي توقفت عن التضاعف وهو يعد القالب الفايروسي الأول في عملية التضاعف، أما القالب الفايروسي الثاني فهو "الوسيط التضاعفي" Rl Replicative intermediate , وهو خيط رايبي جزئي الازدواج Partial dSRNA يحوي العديد من ذيول الخيط المفرد حديثة التولد Nascent product Strands والتي تعرف اختصارا sstails، (الشكل 6). يحتوي الخيطين السالب والموجب على الإشارات Signals المسيطرة على تخصصية وتوقيتات تضاعفهما وتوجد معظم هذه الإشارات عند النهاية 3 لكلا الخيطين فضلا عن احتمال وجودها في مواقع أخرى منهما. يوضح الشكل (7) مخططا مقترحا لتضاعف فايروس تقزم واصفرار الشعير (BYDV) كممثل للفايروسات الرايبية مفردة الخيط موجبة التوجه Sense ssRNA viruses (+). إن آلية تضاعف هذه الفايروسات تمثل أبسط آليات التضاعف إذ لم يسجل احتواء هذه الفايروسات على أية إنزيمات في أغطيتها أو استغلالها لأنزيم الاستنساخ الخلوي المسئول عن استنساخ أنواع الرنا الثلاثة الخلوية RNAS من الدنا الخلوي وهو إنزيم بلمرة الرنا المعتمد على الدنا" DNA dependent RNA polymerase، ودليل ذلك هو عدم تأثر هذه الفايروسات عند معاملتها بالمضاد الحيوي "الاكتينومايسين - د" Actinomycin-D الذي يثبط فعل الإنزيم المذكور، كذلك لم تؤثر إضافة المضادين الحيويين "السايكلوهكسامايد" Cyclohexamide و"الكلورامفينيكول" Chloramphenicol إلى الأنسجة النباتية المصابة بفايروس موزائيك التبغ (TMV) وتلك المصابة بفايروس موت التبغ (TNV) على تخليق البروتين الفايروسي وتضاعف الفايروس مما يدل على أن هذين الفايروسين يستعملان رايبوسومات السايتوبلازم وليس رايبوسومات المايتوكوندريا أو الكلوروبلاستات وذلك لأن هذين المضادين يثبطان عمل هاتين العضيوتين. يتبين مما سبق أن جينومات هذه الفايروسات تعمل بكامل حجمها على أنها رنا مراسل" لتشفير البروتينات الفايروسية ولكن وجد في أنواع منها أن الذي يمثل "الرنا المراسل الفايروسي" Viral mRNA ليس الخيط الأبوي الكامل ولكن واحدة أو أكثر من القطع الجينومية الثانوية موجبة التوجه Sense Subgenomic RNA (+) والتي تخلق من القالب السالب، وتمتلك أنواع من فايروسات عائلتي Potyviridae و Comoviridae بروتينا وظيفيا مرتبطا بالجينوم أطلق عليه مصطلح Genome-linked protein , VPa والذي يستعمله الفايروس بمثابة "بادى" Primer لإطلاق عملية التضاعف، كذلك تعمل أنواع من هذه الفايروسات على تشفير إنزيم "الهيليكيز" Hell Xase مما يعني وجود الية ثانية لإنشاء خيوط الذرية عند التضاعف حيث تمتلك هذه الفايروسات قدرة فصل خيطي الرنا في الشكل التضاعفي بالتحلل المائي للنيكليوسايدات ثلاثية الفوسفات حيث يسهل هذا الإنزيم عملية التضاعف بفصل ازدواجية الشكل التضاعفي، ووجد أن الجينومات الأقصر بمقدار 6 كيلو قاعدة (Kb) عن الجينومات المكونة لانزيم الهيليكيز لا تشفر هذا الإنزيم مما يعني عدم امتلاكها للجين المسئول عن تشفيره، ووجد كذلك أن الفايروسات ذات الجينوم المغطى من النهاية 55 Capped genome تشفر إنزيم "مثيل ترانسفيريز" MTR Methyltransferase , الذي يساهم في تخليق الحامض الرايبي.
تتضاعف الفايروسات الرايبية مفردة الخيط موجبة التوجه ssRNA(+) عادة في السايتوبلازم مرتبطة مع الأغشية الخلوية مستفيدة من بروتينات العائل للمساعدة في تخليق الحامض النووي الرايبي الفايروسي وبذلك لا يمكن لهذه الفايروسات الاستفادة من الية تغطية الرنا المراسل للعائل المسماة Host mRNA capping وهي الالية التي تحصل في النواة عند استنساخ الرنا المراسل من الدنا الخلوي لذلك فهي لا تمتلك إنزيمات مغطاة Capping enzymes أو ربما تمتلك تعاقبا نيوكليوتايديا خاصا يسمح بإجراء عملية الترجمة التي لا تعتمد على آلية التغطية Cap -independent translation، ويتأثر تضاعف هذه الفايروسات بنوع الجينوم الذي تحمله حيث يكون الفرق التركيبي للجينومات عند الطرف 5 هو العامل المهم في بدء التضاعف لأن كل إنزيمات التضاعف الرايبية تبدأ تخليق الذرية من الطرف 5 وبالتالي فان التباين التركيبي لهذا الطرف هو الذي سيحدد الية التضاعف، ووجد أن العديد من أنواع الفايروسات تمتلك جينوم مغلف من النهاية 5 وهو مطابق للتعاقب 7meGPPN الموجود في الرنا المراسلة الخلوية التي تعمل في خلايا العائل مما يعني تماثل آلية تضاعف هذه الفايروسات مع الية استنساخ الرنا المراسلة الخلوية.
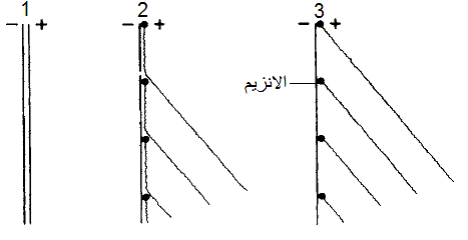
الشكل (6): أشكال الارتباط بين الخيطين السالب والموجب للجينوم الفايروسي.
(1) الشكل التضاعفي Replicative Form , RF حيث يتكامل الخيطين السالب والموجب تماما بكامل طوليهما مع ارتباط كل قواعدهما معا (2) الشكل الوسيط التضاعفي Rl Replicative intermediate , وهو تركيب جزئي الارتباط ترتبط فيه بعض قواعد الخيطين وترتبط كل قطعة مخلقة للخيط الموجب والتي تسمى الذيول مفردة الخيط ss tail وهي الذرية الناشئة الجديدة مع جزيئة من إنزيم البلمرة RdRp المرمز بالدائرة الغامقة. (3) الشكل الوسيط التضاعفي المتوقع وجوده في الخلايا الحية حيث يلاحظ ارتباط جزيئة الإنزيم Rd Rp في نهاية كل خيط جديد وليد حيث يكتمل تخليقه عند النهاية العليا للخيط السالب ثم ينفصل عنه.
الشكل مقتبس من Hull (2002).

الشكل (7): آلية تضاعف فايروس اصفرار وتقزم الشعير BYDV-PAV والتي تمثل آلية تضاعف الفايروسات الرايبية مفردة الخيط موجبة التوجه ssRNA Viruses(+) حيث يتم تحرير الجينوم الفايروسي مفرد الخيط والذي يسلك سلوك الرنا المراسل mRNA ثم يعمل الهيكلين التشفيريين ORF1 و ORF2 بتشفير وحدات إنزيم الربلكيز الفايروسي وتخليقها بواسطة آلية تخليق البروتين Host translation machinery لخلية العائل المصابة وطرحها في الخلية وترتبط وحدات الإنزيم بالجينوم الأبوي بدءا من النهاية 5 وتخلق الخيط السالب الرايبي الذي يعمل كقالب لاستنساخ الذرية ليتم تخليق أفراد الذرية الموجبة من الخيط السالب بنفس الإنزيم ويكون كل فرد جديد مماثل تماما للخيط الأبوي وبنفس طوله ثم يقوم الإنزيم بتخليق القطع الجينومية الثانوية Subgenomic RNAs من الخيط الأبوي والتي تخلق بروتينات الحركة اللازمة لنقل الجسيمات الفايروسية من خلية لأخرى وكذلك بروتينات الكابسيد وبروتينات النقل بالناقل، وتقوم القطعة الجينومية الثانوية الثانية Subgenomic RNA2 بإخماد عملية ترجمة البروتينات من الجينوم الأبوي مما يسبب الانتقال من الإظهار الجيني المبكر إلى الإظهار المتأخر، واخيرا يتم تجميع الجينومات الرايبية الجديدة كاملة الطول Full-length (+) genomic RNAs كل على انفراد مع الوحدات البروتينية المكونة للغطاء لتكوين الفريونات في خلايا النبات العائل.
الشكل مقتبس من Mahy و Van Regenmortel (2008).
ب- تضاعف الفايروسات ذات الحامض الرايبي المفرد سالب التوجه
جميع الفايروسات ذات الحامض الرايبي المفرد سالب التوجه sense ssRNA(-) هي فايروسات مغلفة Enveloped viruses تنتمي لعائلة Rhabdoviridae ويطلق على جينومها مصطلح "الجينوم غير المعدي"Non-infectious genome واكثرها دراسة هما فايروسي " الاصفرار التماوتي للخس" (LNYV) و"التقزم الأصفر للبطاطا" (PYDV) ولا يصبح جينوم هذه الفايروسات لا يصبح معديا إلا بعد استنساخه للخيط الموجب وثبت ذلك عند تلقيح نباتات حساسة بالجينوم العاري لفايروس التماوت الأصفر للخس فلم تحصل الإصابة. تحمل هذه الفايروسات في أغلفتها إنزيم الاستنساخ وهو "الربلكيز" Replicase مرتبطا مع النيوكليوكابسيد الداخلي وثبت ذلك تجريبيا حيث فشل الجينوم السالب في إحداث الإصابة عند إزالة غلاف الفايروس بالمنظفات إذ يعمل هذا الإنزيم على استنساخ الرنا المراسل الفايروسي الأول من الخيط الأبوي السالب وبحجم تعاقبي يكفي لتشفير إنزيم الاستنساخ الفايروسي المتخصص Transcriptase والذي يعمل على استعمال الخيط الأبوي السالب كقالب لاستنساخ الخيط الموجب الثاني الكامل الذي يعمل بدوره قالبا لاستنساخ الخيوط السالبة الجديدة الوليدة (الذرية)، ويبين الشكل (8) مخططات الدورة التضاعفية لهذه الفايروسات.

الشكل (8): إستراتيجية تضاعف فايروسات عائلة Rhabdoviridae الممثلة للفايروسات السالبة التوجه ssRNA(-) (أ) فيروسات الجنس Cytorhabdovirus (ب) فايروسسات الجنس Nucleorhabdovirus.
الشكل مقتبس منHull 2002)).
ج – تضاعف الفايروسات ذات الحامض الرايبي مزدوج الخيط dsRNA Viruses
تنتمي هذه الفايروسات إلى عائلة Reoviridae وأكثرها دراسة هو فايروس التورم الجرحي (WTV) الذي يتكون جينومه من 12 قطعة منفصلة من المزدوج الرايبي dsRNA حيث تعمل كل قطعة منه بشكل مستقل عن الأخرى ولكن بشكل تكاملي، تحمل هذه الفايروسات إنزيم الربلكيز مرتبطا بالنيوكليوكابسيد والذي يعمل على استنساخ الرنا المراسل مفرد الخيط الفايروسي ssmRNA بالية لا تماثل آلية الفايروسات ذات الجينوم الرايبي مفرد الخيط بل تماثل الية الفايروسات ذات الدنا مزدوج الخيط حيث تستنسخ الخيوط الرايبية المراسلة الفايروسية المفردة من القوالب الرايبية المزدوجة ds template RNA والتي تبقى مزدوجة عند التضاعف، ثم تقوم هذه الخيوط المراسلة باستنساخ خيوط جديدة تزدوج لاحقا لتكون الجينومات الجديدة مزدوجة الخيط.
د - تضاعف الفايروسات ذات الجينوم الريبي منقوص الأكسجين مزدوج الخيط dsDNA viruses
تنتمي هذه الفايروسات إلى عائلة Caulimoviridae وهي فايروسات شبه رجعية الاستنساخ Pararetroviruses وتستعمل إنزيم البلمرة Polymerase النباتي الموجود أصلا في خلايا العائل لغرض التضاعف وبتدخل وسيط رايبي" RNA intermediate وباستعمال إنزيم الاستنساخ العكسي, RT Reverse transcriptase , ، وتتلخص آلية تضاعف فايروس موزائيك القرنابيط بتفكك غطائه البروتيني بعد دخوله إلى السايتوبلازم ثم دخول الدنا الفايروسي الحلقي المتحرر إلى النواة عبر مناطق مخصصة في الغشاء النووي والتي تقفل فورا بعد الدخول، ثم يرتبط الدنا مع هستونات العائل ليكون كروموسوما دقيقا Minichromosome يعمل قالبا لاستنساخ قطعتين مستنسختين رايبيتين مفردتي الخيط Transcript RNAs بواسطة الإنزيم الطبيعي الموجود في خلية العائل والمسمى "إنزيم بلمرة الرنا المعتمد على الدنا" DNA dependent RNA polymerase ، وهما القطعة الرايبية 35s RNA والقطعة الرايبية الثانية 19s RNA حيث تعمل القطعة الأولى على تشفير إنزيمي "الاستنساخ العكسي" Reverse transcriptase والذي يطلق عليه اختصارا RT و"الرايبونيوكليز Ribonuclease –H والذي يطلق عليه اختصارا RNase H حيث يتم أولا تخليق قطعة دنا مفردة سالبة التوجه من القطعة الرايبية 35s RNA بواسطة إنزيم الاستنساخ العكسي والذي يخلقها من الموقع المحصور بين النيوكليوتايدتين 500-700 من النهاية 5 للقطعة الرايبية المذكورة حيث يوجد تعاقب نيوكليوتايدي تكاملي مع النهاية 3 للرنا الناقل tRNA، فيما يعمل إنزيم RNase H على إزالة الجزء الرايبي RNA-moiety من "مزدوج الدنا- الرنا" DNA: RNA duplex وتظهر مواقع غنية بالبيورين Purine-rich regions لتصبح بمثابة "بوادى" Primers لتخليق خيوط الدنا المفردة الخيط موجبة التوجه ثم وبواسطة إنزيم الاستنساخ العكسي يزدوج الخيطين الموجب والسالب ليكونا الجينوم الفايروسي المزدوج المماثل للجينوم الأبوي، يبين الشكل (9) الية تضاعف فايروس موزائيك القرنابيط (CaMV) الممثل لهذه الفايروسات.
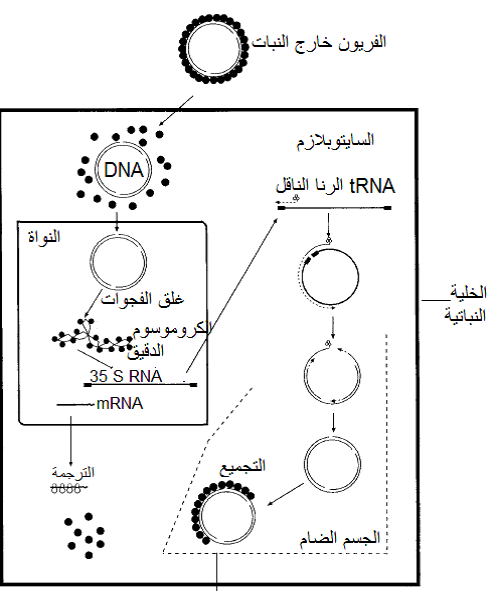
الشكل (9): مخطط الدورة التضاعفية لفايروس موزائيك القرنابيط (CaMV) الممثل لعائلةCaulimoviridae .
الشكل مقتبس من Hull (2005).
هـ- تضاعف الفايروسات ذات الجينوم الرايبي منقوص الأكسجين مفرد الخيط ssDNA viruses
تنتمي هذه الفايروسات لعائلة Geminiviridae وهي ذات جينوم حلقي بحجم 2.5-3 كيلو قاعدة هو موزع بين جسيمتين توأميتين أيزومتريتين، تتضاعف هذه الفايروسات وفق "نظام التضاعف الحلقي اللفائفي" Rolling Circle replication System والذي يعمل الدنا الأبوي الموجب مفرد الخيط سلوك قالب لتخليق الدنا المفرد السالب وتكوين الشكل التضاعفي المزدوج ds-replication form وذلك بمساعدة جزيئة حامض رايبي RNA حيث يتم استنساخ الخيط الجديد من الخيط السالب وهو في حالة ازدواجيته مع الخيط الموجب بدون أن ينفصل عنه، ويبتدئ الاستنساخ بواسطة ثلم في موقع معين على الخيط السالب ليتم إنتاج الخيط الموجب بطول الجينوم الأبوي ثم تربط نهايتيه لإعطاء الشكل الحلقي المغطى Circular encapsidation form وكما مبين في الشكل (10) لم يلاحظ تشفير هذه الفايروسات لأية إنزيمات فايروسية مبلمرة للدنا DNA polymerase لذا من المحتمل استعمالها لإنزيمات البلمرة الخاصة بالعائل لغرض تضاعفها.
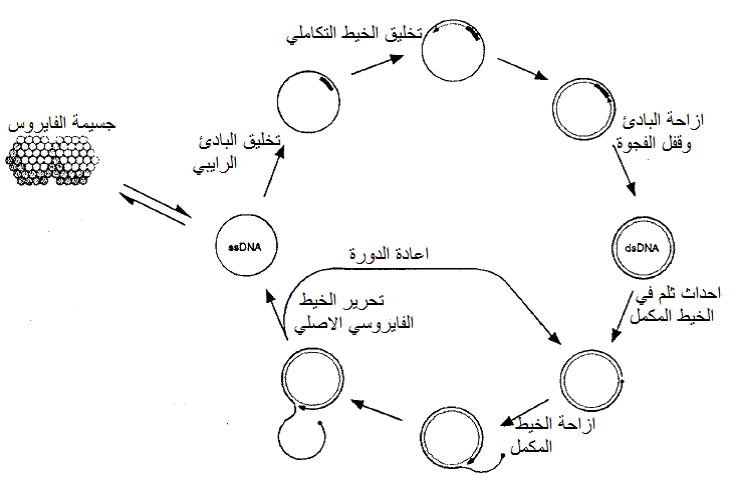
الشكل (10): إستراتيجية تضاعف فايروسات عائلة.Geminiviridae
الشكل مقتبس منHull (2002).
3.2. مرحلة تجميع الجسيمات الفايروسية
مرحلة تجميع الجسيمات الفايروسية Assembly of Virus particles هي المرحلة التي تعقب التضاعف وإنتاج الذرية والتي يتم فيها ارتباط الجينوم الوليد الجديد مع وحدات بروتين الكابسيد لبناء الجسيمة الكاملة "الفريون" وهي تحدث في مواقع معينة في السايتوبلازم عادة حيث تتكون أجسام بروتينية كثيفة تسمى "الفايروبلازم" Viroplasim وهي نوع من الأجسام الضامة الكبيرة التي يمكن مشاهدتها بالمجهر الضوئي، وتتباين فايروسات النبات في مواقع وطبيعة تجميعها فمثلا يتم تجميع فايروس الموزائيك الأصفر للشلغم (TYMV) في حويصلات عنقودية Clustered Vesicles موجودة على أسطح الكلوروبلاستات وذلك عند بروز خيط الحامض النووي منها وقد يحصل تجميع بعض الفايروسات في النواة. إن التجميع هي عملية تلقائية تحدث كلما التقى الحامض النووي الفايروسي بالوحدات البروتينية بل وحتى مع الوحدات البروتينية لنوع فايروسي آخر أحيانا وهذا ما يحصل في الإصابات الخليطة حيث تسمى هذه الظاهرة "اعادة الارتباط" Recombination او Encapsidation. يطلق مصطلح "الفايروس المتجانس" Homologous virus عند ارتباط الجينوم مع الوحدات البروتينية الخاصة به فيما يطلق مصطلح "الفايروس المتغاير" Heterologous Virus عند ارتباط الجينوم مع الوحدات البروتينية لفايروس اخر. بعد انتهاء عملية التجميع تتكون الفايروسات الكاملة او الناضجة Intact viruses, Virions or Mature virusesإلى الخلايا المجاورة للخلايا المصابة فيما يبقى القسم الأخر من هذه الجسيمات الكاملة الوليدة في الخلايا المصابة التي نشأت فيها وكأنها جسيمات سابتة مهيأة للنقل إلى عائل جديد سواء بالناقلات أو بوسائل النقل الأخرى كي تضمن الفايروسات بقائها في البيئة، وبذلك يمكن أن نطلق على هذه الجسيمات مجازا مصطلح "الجراثيم الفايروسية" Virus spores.
أ- تجميع الفايروسات العصوية
جاءت أغلب المعلومات عن تجميع هذه الفايروسات من دراسة فايروس موزائيك التبغ (TMV) حيث تخلق الوحدات البروتينية البنائية للكابسيد من قبل الرايبوسومات وتتجمع بشكل وحدات منفردة "موحودات" Monomers وتطرح في السايتوبلازم لتتكون تحت ظروف خاصة من حرارة منخفضة نسبيا وقوة أيونية واطئة وأس هيدروجيني قاعدي التراكيب الثنائية Dimers ثم الثالثية Trimers وبذلك يتكون "البروتين أي" Protein-A والذي يشكل الوحدة Pentamer ثم تتجمع عدة تراكيب خماسية معا لتكوين القرص المزدوج Double helx وكما مبين في الشكل (11) وهو أهم تجمع بروتيني فعال قادر على الارتباط مع الحامض النووي، ويتكون هذا القرص في فايروس موزائيك التبغ من 34 وحدة بروتينية ويتم التجميع بارتباط كل قرصين مع بعضهما حول الحامض الرايبي ابتداءا من النهاية 5 باتجاه النهاية 3, وتمتلك الأقراص المزدوجة قدرة عالية على الارتباط مع الحامض النووي بسرعة تزيد بمقدار مائة ضعف عما يستطيعه "البروتين أ. لا يتكون الشكل الحلزوني المميز للجسيمات العصوية الا تحت الظروف الحامضية حيث يكون بناء الغطاء متماسكا عند الأس الهيدروجيني بقيمة 6 بواسطة الأواصر الكهربائية Electrovalent bonds والأواصر الكاره للماء Hydrophobic bonds ,ولتفسير طريقة تجميع الأقراص مع الحامض النووي فقد اقترح تحول القرص المزدوج الى الشكل المعروف بمصطلح "الفكة القافلة" Lock Washer أو يسمى "الحلزون ثنائي الدورة" Two turn helix. إن ارتباط الحامض النووي بالوحدات البروتينية يجعل الكابسيد أكثر ثباتا وذلك بسبب قدرة الحامض النووي على تغيير الوسط الكيموكهربي داخل الجسيمة وبذلك تبقى الوحدات البروتينية ثابتة حتى في الوسط القاعدي. لوحظ إمكانية ارتباط الوحدات البروتينية مع بعضها وتكوين الحلزون دون وجود الحامض النووي، أي تكوين ما يعرف بمصطلح "الجسيمة الفارغة" Empty particle إلا أنه بوجود الحامض النووي فان التجميع يحصل بسرعة أكبر، ولوحظ وجود تعاقب نيوكليوتايدي طرفي عند النهاية 5 بحجم 40 نيوكليوتايدة ذو ألفة كبيرة مع أول قرص مزدوج، وعند حدوث الارتباط فأن كل وحدة بروتينية واحدة ترتبط مع ثلاث نيوكليوتايدات.
ب– تجميع الفايروسات الأيزومترية
لا توجد معلومات كثيرة عن تجميع هذه الفايروسات مقارنة بالفايروسات العصوية وأكثر المعلومات المتوفرة عنها جاءت من الدراسات التي أجريت على فايروسات عائلة Bromoviridae وخاصة فايروس موزائيك نجيل البروم (BMV) والتي يعتمد تجميعها على الأواصر الهيدروجينية القائمة بين مجاميع كاربوكسيل الوحدات البروتينية المتجاورة التي تعمل على وضع الوحدات البروتينية بدقة في مواضعها الصحيحة في البلورة فضلا عن الأواصر الكهربائية Electrovalent links القائمة بين الوحدات البروتينية والحامض النووي وأيد ذلك تماسك هذه الوحدات تحت الظروف الحامضية التي تسمح بتكوين هذه الأواصر، ووجد أنه عندما تصبح مجاميع الكاربوكسيل في وسط متعادل فإنها تتأين مما يؤدي إلى حصول تنافر بين كل وحدتين بروتينيتين متجاورتين وينتج عنه انتفاخ الجسيمة الفايروسية ولكنها تبقى متماسكة بواسطة الأواصر الكهربائية ولكن بوجود أيونات الكالسيوم والصوديوم فإنها تعمل على تفكيك الأواصر الكهربائية فتتفكك الوحدات البروتينية، ولوحظ أن وجود كاتايونات ثنائية أو متعددة الارتباط Divalent or Polyvalent Cations يمنع تأين مجاميع الكاربوكسيل في الوسط المتعادل كما نجح الباحثون تجريبيا في إعادة تجميع الوحدات البروتينية المفككة وبناء الهيكل الفايروسي ثانية بمزج النسب الصحيحة من الوحدات البروتينية مع الجينوم في محلول متعادل ملحي لكلوريد الصوديوم بتركيز 0,5 مولر وإضافة أيونات المغنيسيوم المذابة بشكل كلوريد المغنيسيوم في محلول منظم بتركيز 0.05 حيث تعمل هذه الأيونات جسرا بين مجاميع الكاربوكسيل لتثبت الوحدات البروتينية في أماكنها. يمكن لبعض فايروسات Bromoviruses تكوين جسيمات بلورية فارغة ذات معامل ترسيب S52 والتي يطلق عليها "المكون الكاذب القمي" Pseudo-top-Component وأطلقت عليها هذه التسمية لأنها تطفو في أنبوبة الانتباذ عند تنقيتها بسبب خفتها النسبية لخلوها من الحامض النووي.
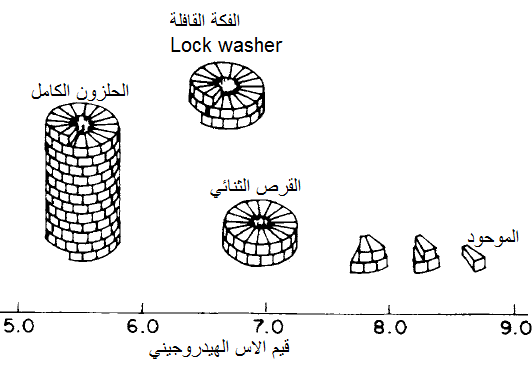
الشكل (11): مخطط لآلية تجميع الكابسيد الحلزوني داخل الخلية وعلاقة ذلك بقيم الاس الهيدروجيني للخلية حيث يبدأ تجمع الوحدات البروتينية بشكل "موحود" عند الاس الهيدروجيني 8.8 تقريبا ثم يتكون التركيب الثالثي ثم الخماسي لتكوين القرص المزدوج ثم انفتاحه بشكل "الفكة القافلة" Lock-washer وهو التركيب الأساسي لتكوين الحلزون والذي يكون ثابتا عند الأس الهيدروجيني 5,5 - 6.
الشكل مقتبس منHull 2002)).
ج- تجميع وتغليف الفايروسات المغلفة
يتم تجميع الكابسيد مع الحامض النووي التكوين النيوكليوكابسيد لهذه الفايروسات بالطريقة ذاتها التي ذكرت للفايروسات العصوية والأيزومترية وذلك حسب نوع الفايروس المغلف أما بناء الغلاف الخارجي الليبيدي المحيط بالكابسيد فانه يتم بآلية اكتساب ذلك الغلاف من الأغشية الخلوية للعائل وتحديدا من الغشاء النووي الداخلي أثناء مغادرة النيوكليوكابسيد الفايروسي لنواة خلية العائل بعد إتمام التضاعف وتجمع الجسيمات الفايروسية في المساحة النووية المحيطية Perinuclear Space أي أن هذه الفايروسات تكتسب غلافها الليبيدي من أغشية الشبكة الأندوبلازمية لخلايا العائل أثناء عبورها لها إلى السايتوبلازم بآلية "التبرعم" وهي الآلية المقترحة والأكثر قبولا لتفسير الكيفية التي تغلف بها الفايروسات المغلفة وخاصة تلك التابعة لعائلة Rhabdoviridae ودليل ذلك هو تشابه تركيبة الغلاف الفايروسي تماما مع تركيبة أغشية خلايا العائل.
4.2. آلية تخليق البروتينات الفايروسية داخل الخلايا النباتية المصابة
تعتمد عملية التضاعف الفايروسي وبغض النظر عن نوع الفايروس على إنتاج نوعين أساسيين من البروتينات وهما إنزيمات التضاعف الفايروسي وبروتينات الكابسيد ويتم ذلك داخل الخلايا الحية المصابة باستعمال نفس الية تخليق البروتينات الخلوية المعتمدة على "معقد الرايبوسوم - الرنا المراسل – والرنا الناقل"، ويطلق على عملية تخليق البروتين "الترجمة" Translation وتعني بناء البروتين بتعاقب معين للأحماض الأمينية يحدده تعاقب النيوكليوتيدات في الحامض النووي الفايروسي والترجمة هي جزء من عملية التضاعف الكلية التي تضم ثلاث مراحل هي: التضاعف Replication وتعني مضاعفة الجينوم الفايروسي سواء كان مفردا أو مزدوجا لتكوين جينومات جديدة ثم مرحلة الاستنساخ Transcription وتعني استنساخ خيط الرنا المراسل mRNA من الجينوم الفايروسي وأخيرا مرحلة الترجمة Translation وهي انتاج البروتينات الفايروسية بنوعيها الوظيفي والتركيبي في الرايبوسومات اعتمادا على الشفرة التي يحملها الرنا المراسل.
تمر عملية ترجمة البروتينات الفايروسية بخمسة مراحل هي (1) ارتباط حامض أميني معين مع الرنا الناقل tRNA المخصص له (2) حصول عملية "الابتداء" Initiation أي البدء بتخليق البروتين بارتباط أول رنا ناقل مع الكودون المبدئ nitiation Codon الموجود في الرنا المراسل mRNA وذلك بعد ارتباط الأخير مع الرايبوسوم لتكوين معقد "الرايبوسوم – الرنا المراسل" mRNA - Ribosome Complex (3) بلمرة الأحماض الأمينية المتعاقبة على هذا المعقد وتكوين التركيب الأولي للبروتين وهو التعاقب الخيطي غير المتفرع للأحماض الأمينية المتعاقبة المرتبطة مع بعضها بالأواصر الببتيدية (4) تفكك معقد "الرايبوسوم - الرنا المراسل.
3. حركة الفايروسات في النباتات
هي المرحلة الثالثة من مراحل الإصابة والتي تعقب مرحلة التضاعف الفايروسي وهي تعد مرحلة أساسية لاكتمال الإصابة الفايروسية فمن دونها لا تكتمل الإصابة حتى لو نجح الفايروس بالتضاعف داخل الخلايا، أظهرت الدراسات المبكرة التي أجريت على حركة الفايروسات في النبات أنها تتحرك جهازيا في أنسجة اللحاء وثبت ذلك تجريبيا بتجارب التركيب حيث ظهرت الأعراض في الطعوم السليمة المطعمة على أصول مصابة وبينت الدراسات التي اعتمدت طريقة قطع وإتلاف اللحاء بطريقة التحليق الحراري Heat girdling طبيعة اتجاه وسرعة تحرك الفايروسات من الخلايا المصابة باتجاه الأنسجة السليمة حيث تتحرك الفايروسات التي تصيب النباتات جهازيا أولا ببطء عبر الخلايا النباتية ثم إلى نسيج اللحاء محمولة مع الغذاء فيما تتحرك القلة من الفايروسات عن طريق أوعية الخشب ويكون اتجاه حركتها أولا نحو الجذور ثم إلى الأوراق الحديثة في قمة النبات لتتحرك بعدها نزولا إلى بقية أجزاء النبات وقد أيدت الدراسات التي أجريت باستعمال المجهر الالكتروني وجود الحركتين البطيئة عبر البلازموديزماتا والسريعة خلال اللحاء بمشاهدة الجسيمات الفايروسية فيهما وذلك عند دراسة أنماط الحركة في نوعين من الأعراض وهما الموزائيك والاصفرار حيث تحددت مناطق الإصابة في الأعراض الأولى بنوع التعريق في الأوراق Leaf vasculature مما يدل على نقل الفايروس عبر الخلايا ثم بالأنسجة الوعائية فيما دلت أعراض الاصفرار على انتشار الفايروس حتما بالأنسجة الوعائية حيث أن فايروسات الاصفرار تصيب اللحاء وتتحرك فيها، وهكذا ولكي تكتمل الإصابة الجهازية يتوجب على الفايروس النباتي أن يتحرك أولا حركة بطيئة عبر الخلايا ثم تعقبها حركة سريعة وطويلة عبر الأنسجة الناقلة وخاصة اللحاء ثم يعود ثانية إلى الحركة البطيئة لإصابة خلايا جديدة وإنشاء مواقع إصابة جديدة في النبات.
1. الحركة البطينة (الحركة بين الخلايا)
تحصل الحركة البطيئة (الحركة بين الخلايا) Slow or Cell-to-Cell movement بتحرك الفايروسات الكاملة أو جينوماتها داخل الخلية المصابة في السايتوبلازم وكذلك عبر الأغشية الخلوية بالنسبة للفايروسات المتضاعفة فيه أو من النواة إلى السايتوبلازم بالنسبة للفايروسات المتضاعفة في النواة ويعتقد أن هذه الحركة تتم بظاهرة الضغط الانتشاري وحركة السايتوبلازم الدورانية وبعد اكتمال تضاعف الفايروس داخل الخلية وامتلائها بالأفراد الجديدة ثم تبدأ هذه الأفراد بالحركة من خلية لأخرى عبر الروابط السايتوبلازمية الرابطة بين سايتوبلازم كل خليتين متجاورتين والمسماة "البلازموديزماتا" Plasmodesmata وهي قنوات سايتوبلازمية مبطنة بالأغشية البلازمية تمتد عبر جدران خلايا النبات، (الشكلين 12 و 13 ) لتسهل الانتشار بين الخلوي للجزيئات الحيوية الخلوية وخاصة البروتينات والأيونات. يبلغ معدل أقطار البلازموديزماتا في النباتات بحدود 3 نانومتر وهو قطر لا يكفي لعبور الجسيمات الفايروسية التي تتراوح معدلات أقطارها بين 10-100 نانومتر، (الشكل 14) لذلك لا بد من حدوث تحوير لها كي تتوسع لتسامح للجسيمات الفايروسية من العبور خلالها حيث تلعب بروتينات الحركة MP و Movement proteins التي تشفرها الفايروسات دورا في تحوير البلازموديزماتا والارتباط بالجسيمات الفايروسية لتمريرها عبر هذه القنوات. وقد أثبتت الدراسات التي أجريت على فايروس موزائيك الداليا (DMV) والذي يبلغ قطر جسيماته 50 نانومتر ذلك حيث أظهرت صور المجهر الالكتروني وجود عدد من البلازموديزماتا المحورة التي أصبحت بشكل شبه أنبوبي وهي ممتلئة بصف مفرد من جسيمات الفايروس، ولقد فسرت عدة آليات لتفسير الكيفية التي تحور بها البلازموديزماتا لتصبح مهيأة لعبور الفايروسات وبالاستعانة ببروتينات الحركة مع العديد من أنواع الفايروسات والتي يوضحها الشكل (15)، ويبين الجدول (3) أنواع من بروتينات الحركة بين الخلايا والخاصة بعدد من أنواع الفايروسات.
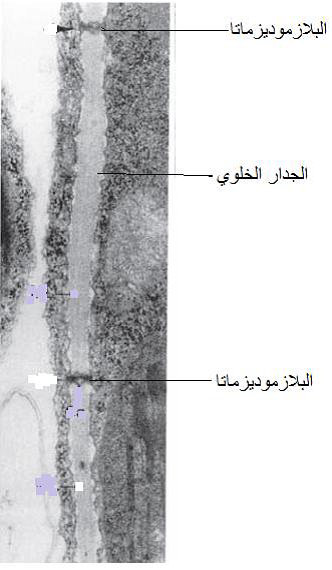
الشكل (12): صورة بالمجهر الالكتروني يبين مواقع البلازموديزماتا في الجدار الخلوي الفاصل بين خليتين.
الشكل مقتبس من Hull 2009)).
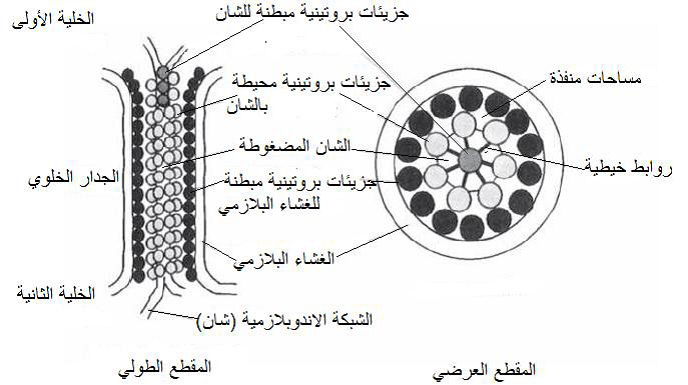
الشكل (13): التركيب التشريحي للبلازموديزماتا بالمقطعين الطولي والعرضي، (الرمز "شان" يعني الشبكة الاندوبلازمية).
الشكل مقتبس من Hull 2009)).
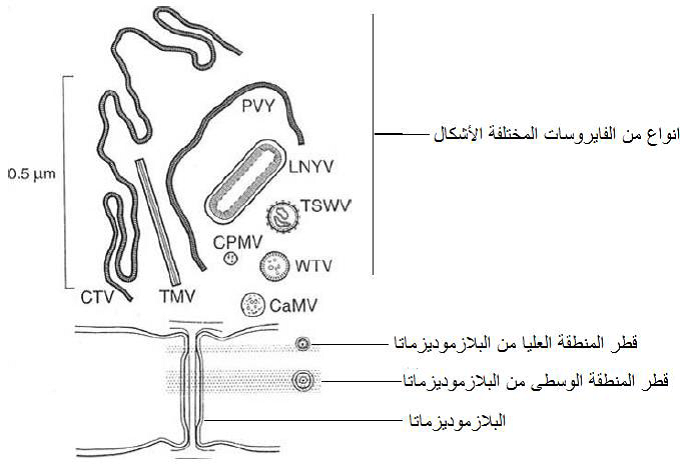
الشكل (14): مخطط يبين صغر حجم قطر البلازموديزماتا الطبيعية والذي لا يزيد عن 3 نانومتر، مقارنة بحجوم عدد من انواع الفايروسات المختلفة الاشكال.
الشكل مقتبس من Hull (2009).
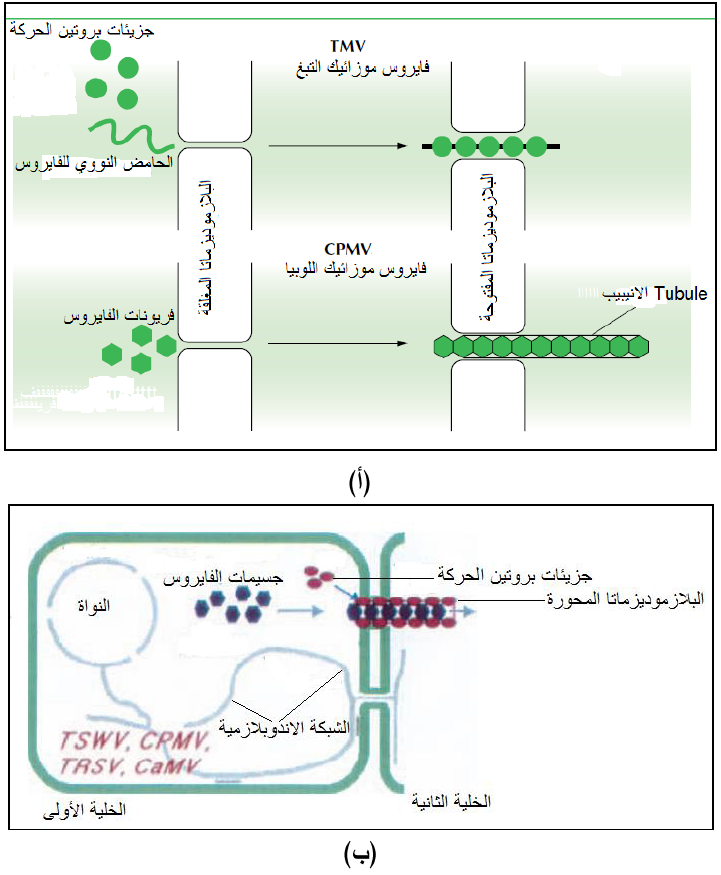
الشكل (15): (أ) نموذج مقترح لألية عمل بروتينات الحركة لتسهيل عبور الفايروسات العصوية والايزومترية عبر البلازموديزماتا بعد توسعتها بتلك البروتينات، حيث يظهر الشكل العلوي أن جزيئات بروتين الحركة ترتبط بالحامض النووي لفايروس موزائيك التبغ الممثل للفايروسات العصوية وليس بالفايروس الكامل وتمرره عبر البلازموديزماتا، أما الآلية الثانية فهي اصطفاف جزيئات بروتين الحركة بشكل أنيبيب Tubule في فجوة البلازموديزماتا وتوسعتها لتمر منها الجسيمات الفايروسية الأيزومترية الكاملة كما موضح مع فايروس موزائيك اللوبيا. (ب) نموذج لحركة أربعة أنواع من الفايروسات الأيزومترية عبر البلازموديزماتا حيث يتم إقحام تركيب أنبوبي قصير مكون من بروتين الحركة في تجويف البلازموديزماتا لغرض توسعته للسماح للجسيمات الفايروسية بالعبور خلالها وهناك أدلة على دور الشبكة الأندوبلازمية في هذه الحركة، (مختصرات اسماء الفايروسات مبينة داخل الشكل).
الشكل مقتبس من Cann (2005) و Hull (2009).
وتمت دراسة دور بروتين الحركة في نقل الفايروسات عبر الخلايا بإتباع الطرق المناعية الخلوية Immunocytological methods التي تعتمد استعمال أضداد بروتينات الحركة والكشف عن وجودها مصليا باستعمال طريقة البصمة الغربية Western blot method حيث تم الكشف عن وجود هذه البروتينات في البلازموديزماتا المحورة، كما تحدث تحويرات تركيبية في البلازموديزماتا لغرض توسعة تجويفها عن طريق تكوين الأنيبيبات البلازموديزماتية Plasmodesmata tubules والتي لوحظت في العديد من أنو اع النباتات المصابة بفايروسات Comoviruses و Nepoviruses و Badnaviruses ،Tospoviruses، ويشفر فايروس موزائيك اللوبيا (CpMV) بروتينين بحجم 48 و 58 كيلودالتون المسئولين عن تكوين الاثيبيبات التي تعمل علي توسعة الشكل الأنبوبي للبلازموديزماتا وبالتالي تعمل هذه الأنيبيبات تحوير التجويف البلازموديزماتي أي زيادة حجم حدود السعة البلازموديزماتية" Plasmodesmal size exclusion limit, SEL بعبور جزيئات أكبر بكثير من تلك التي تقوم بتمريرها في الحالة الطبيعية.
وهناك إشارات إلى حدوث آلية معقدة لعبور عدد من أنواع الفايروسات بشكل حامض نووي عاري غير فريوني مرتبط مع بروتين الحركة مباشرة حيث يتكون "المعقد النيوكليوبروتيني غير الفريوني" Non-Virion nucleoprotein complex وليس كما هو مقترح في الألية السابقة بارتباط بروتين الحركة مع بروتين الكابسيد وقد لوحظ ذلك مع فايروس موزائيك وتقزم الفاصوليا (BDMV) ذو جينوم من النوع ssDNA والذي يتضاعف في النواة وعليه فان الفايروس يحتاج إلى نوعين من بروتينات الحركة وهما البروتين BV1 الذي ينقل الجينوم من النواة إلى السايتوبلازم والبروتين BC1 الذي ينقله عبر البلازموديزماتا الي الخلايا المجاورة.
تسبب الحركة البطيئة انتشارا موضعيا للفايروس في النبات إذ لا يتحرك بواسطتها عبر الخلايا لأكثر من 0,2 ملم يوميا كمعدل عام لكل الفايروسات ويعني ذلك أن الفايروس يحتاج إلى عدة أيام للانتشار في الورقة النباتية الواحدة ويتحكم في سرعة هذه الحركة مقدار تضاعف الفايروس داخل الخلية وبتناسب طردي فكلما زاد مقدار التضاعف زادت سرعة هذه الحركة.
أ- الجينات الفايروسية المسئولة عن الحركة البطيئة للفايروسات
ساعدت تقانة الاستنساخ الجزيئي Molecular Cloning في الكشف عن الجينات المسئولة عن تشفير بروتينات الحركة في الفايروسات فقد عرف الجين المشفر لبروتين الحركة في فايروسات Tobamoviruses وهو بحجم 30 كيلوداتون وذلك بدراسة طفرات من فايروس موزائيك التبغ (TMV) حساسة حراريا وخاصة الطفرة LS1 التي تفقد قدرتها على الحركة بين الخلايا عند تعرضها إلى درجات حرارية عالية نسبيا، ووجد أن الفرق الوحيد بين السلالة البرية للفايروس والطفرة LS1 هو حامض أميني واحد استبدل في تعاقب بروتين الحركة، كذلك سجل وجود الجين a3 الذي يشفر بروتين الحركة المسمى 3a protein في القطعة الجينومية الثالثة RNA3 وهي ثنائية التشفير Dicistronic في فايروسات Bromoviruses المكون جينومها من ثلاث قطع هي RNA1 و RNA2 و RNA3، ووجد أن بروتين غطاء هذه الفايروسات ضروري للنقل البعيد عبر اللحاء والنقل البطيء عبر الخلايا. وتشفر جينومات فايروسات Potyviruses بروتينا كبيرا Polyprotein والذي يسمى HC-Pro وهو يلعب دورا في نقل هذه الفايروسات عبر الخلايا وفي النقل البعيد لها داخل النباتات. وتمتلك فايروسات Potexviruses و Carlaviruses و Hordeiviruses وبعض أنواع فايروسات Furoviruses مجموعة من ثلاثة جينات متداخلة Overlapping genes ويطلق على القطعة الجينومية التي تحمل هذه الجينات مصطلح "القطعة الجينومية ثلاثية الجين" , TGB Triple gene block وهي تشفر بروتينات الحركة البطيئة والسريعة لهذه الفايروسات. أما الفايروسات التوأمية Geminiviruses ذات الجينوم منقوص الأكسجين المفرد ssDNA فان بعض أنواعها هي أحادية الجينوم Monopartite genome وهي تمتلك الجين CP وهو المسئول عن تشفير بروتين الغطاء وهو ذات البروتين المسئول عن حركة هذه الفايروسات في النباتات، أما أنواعها الأخرى ثنائية الجينوم Bipartite genome فهي تتكون من قطعتين جينوميتين متماثلتي الحجم وهما DNA-A و DNA-B والقطعة الأخيرة هي التي تحمل جينات تشفير بروتينات الحركة حيث تحمل الجينين BC1 و BV1 المسئولين عن ذلك.
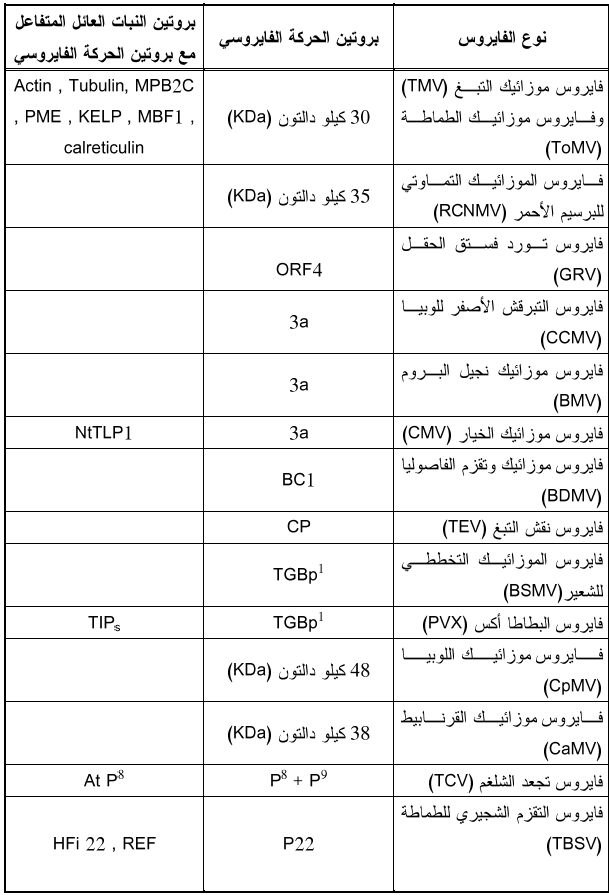
الجدول (3): البروتينات اللازمة لنقل الفايروسات عبر خلايا العائل
2. الحركة السريعة (حركة المسافات الطويلة)
الحركة السريعة أو حركة المسافات الطويلة Quick or long-distance movement هي حركة الفايروسات إلى الأنسجة والخلايا البعيدة عن منطقة دخول الفايروس في النبات، وهي الحركة المسئولة عن نجاح الإصابات الفايروسية الجهازية وتبدأ هذه الحركة بعد نجاح الفايروس في اجتياز عدة خلايا بواسطة الحركة البطيئة ليصل إلى أوعية اللحاء في الورقة ثم ينتشر بسرعة في عروقها ويكتمل انتشاره فيها خلال ثلاثة أيام تقريبا وحسب نوع الفايروس والنبات، ثم يبدأ الفايروس بالحركة باتجاه الجذور محمولا مع الغذاء المنقول باللحاء مستغلا آلية نقل الغذاء ثم يتجه بعد ذلك إلى المناطق العليا من النبات لتكتمل الاصابة الجهازية بعد أسبوعين – ثلاثة أسابيع في معظم النباتات العشبية، (الشكل 16) ولقد شوهدت جسيمات العديد من فايروسات النبات بواسطة المجهر الالكتروني في الأنابيب الغربالية وفي ثقوب صفائحها وتصل سرعة نقل الفايروس في هذه الحركة إلى عدة سنتمترات في الساعة وحسب نوع الفايروس والنبات فمثلا تصل سرعة نقل فايروس موزائيك التبغ في الأنسجة المصابة إلى 8 سم/ساعة، كما لوحظت بعض أنواع الفايروسات تتحرك في اللحاء بعكس حركة الغذاء، وجد أيضا أن هناك قلة من أنواع الفايروسات تتحرك في أوعية الخشب. ولكي تكون الحركة السريعة كفؤة فأن ذلك يتطلب امتلاك الفايروس لقدرة الدخول إلى اللحاء أو الخشب ثم الخروج من هذه الأنسجة بذات كفاءة الدخول. درست حركة الفايروسات في الأوعية الناقلة باعتماد تقانات عديدة واعتمدت الدراسات المبكرة على أخذ عينات من أنسجة النبات الملقح بالفايروس عند فترات زمنية معينة بعد التلقيح ثم يكشف عن الفايروس باستعمال النباتات الكاشفة لمعرفة مواقع وصول الفايروس في أنسجة النبات المصاب كما حصل عند متابعة حركة فايروس موزائيك القرنابيط (CaMV) في نبات الشلغم حيث وجد أن هذا الفايروس لا يستطيع الوصول إلى الأنسجة الزهرية في مرحلة إزهار النباتات وتسمى هذه الظاهرة "المقاومة التطورية أو النشوئية" Developmental resistance وهي المقاومة المرتبطة بتطور النبات من مرحلة النمو الخضري إلى النمو الزهري ولوحظت الظاهرة ذاتها مع فايروس موزائيك وتقزم الفاصوليا (BDMV) عند إصابته لنبات الفاصوليا حيث يتوقف خروجه من اللحاء خلال المراحل المبكرة للإزهار ولكن ليس خلال النمو الخضري أو بعد انتهاء الإزهار، كما استعملت طريقة تحليق النبات Girdling لدراسة هذه الحركة وإثبات أن الفايروسات تتحرك باتجاه حركة الغذاء في أوعية اللحاء محمولة في الغذاء لذلك يطلق على ذلك مصطلح "النقل بالأيض الضوئي Photo assimilate transmission أي إتباع الفايروسات لنمط حركة الغذاء من مصدر إنتاجه وصولا إلى الأنسجة المستقبلة له Source -to- Sink pattern، أما التقانات الحديثة التي استعملت لدراسة الحركة فهي الدراسات الجينية باستعمال جينات معلمة إشعاعيا يطلق عليها الجينات المُخبرة Reporter gene إذ يتم إدخال جين معلم Tagged virus في نسيلة فايروسية وبذلك تسهل متابعة ذلك الفايروس عند حركته في النبات، واستعملت هذه التقانة لمتابعة حركة فايروس نقش التبغ (TEV) في النبات باستعمال الجينين المعلمين GUS و GFP حيث لوحظ بقاء الفايروس في خلايا البشرة لمدة 12 ساعة بعد الإصابة لإتمام نزع الغطاء البروتيني والتضاعف ثم بدأ بالتحرك ليجتاز خلية واحدة كل ساعتين أعقبها بدء الحركة الطويلة حيث كانت أول الخلايا التي أظهرت نشاطا للجين GUS والبعيدة عن منطقة الإصابة الأولية هي الخلايا القريبة من الأنابيب الغربالية للحاء ثم أعقبها خروج الفايروس منها إلى الخلايا المرافقة وبارانكيما اللحاء.
لكي يتم الفايروس حركته السريعة في النبات المصاب فانه يحتاج (1) إظهار (تشفير) بروتينات الحركة اللازمة لتسهيل الحركة البطيئة (2) تضاعف الفايروس ووصول تركيز جسيماته في منطقة الإنتاج إلى التركيز الحرج Critical titer اللازم لضخ الفايروس بشكل كاف إلى اللحاء (3) الوقت اللازم للجسيمات الفايروسية للحركة من خلايا البشرة ثم عبر خلايا الميزوفيل وإلى الأوعية الناقلة.
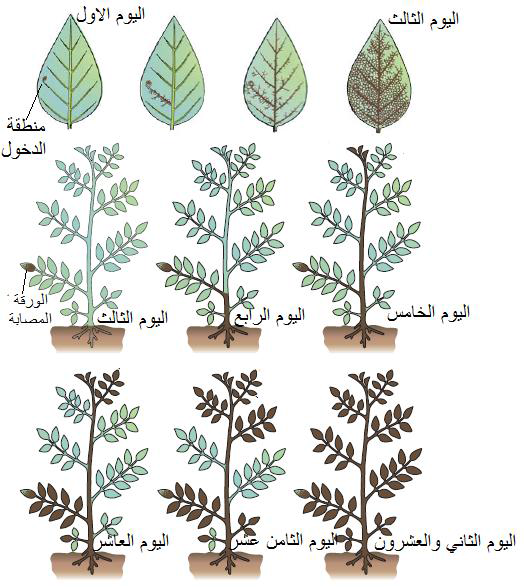
الشكل (16): المسار المعتاد للفايروسات التي تصيب النباتات العشبية جهازيا من نقطة الدخول في الورقة العليا اليسرى لحين اكتمال الاصابة في النبات الادنى الايمن، يلاحظ ان الفايروس يتجه اولا الى الجذور في اليوم الرابع من الاصابة حيث يوضح اللون البني مسار الفايروس في النبات ثم يتحرك صعودا الى بقية اجزاء النبات، والتوقيتات المثبتة تقريبية تتباين حسب نوع النبات والفايروس وظروف الاصابة.
الشكل مقتبس من Agrios (2005).



|
|
|
|
15 نوعا من الأطعمة تساعدك على ترطيب جسمك خلال موجة الحر
|
|
|
|
|
|
|
دول عربية تقرر قطع الكهرباء لساعات محددة يوميا بسبب الحرارة
|
|
|
|
|
|
|
بالصور: بمناسبة عيد الغدير الاغر.. قراءة خطبة النبي الأكرم (ص وآله) بالمسلمين في يوم (غدير خم)
|
|
|