

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء التناسقية

الكيمياء الاشعاعية والنووية
The Mannich Reaction
المؤلف:
William Reusch
المصدر:
Virtual Textbook of Organic Chemistry
الجزء والصفحة:
............
5-8-2018
4031
The Mannich Reaction
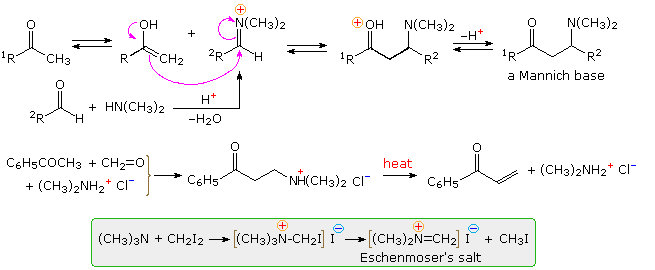
The Mannich reaction is similar to a crossed aldol reaction in that a nucleophilic enol-donor forms a carbon-carbon bond to an electrophilic iminium-acceptor. This assembly is outlined at the top of the following diagram, using a methyl ketone as the enol precursor and an aldehyde iminium electrophile. Formaldehyde is a commonly used aldehyde reactant, as shown in the example below the mechanism. The Mannich base product is a β-aminoketone, usually formed as a mineral acid salt. These bases find use as stable precursors of reactive α,β-unsaturated carbonyl compounds, as illustrated in the same example. Eschenmoser's salt is a particularly useful source of formaldehyde for Mannich reactions.
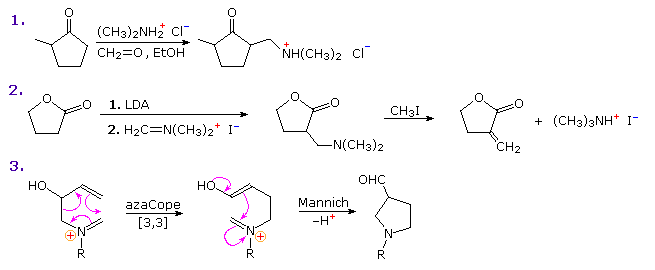
The first is a straightforward reaction involving the kinetically favored enol of a cyclic ketone. The second shows the reaction of Eschenmoser's salt with a preformed lithium enolate. Such reactions produce the free base directly. In order to effect the β-elimination of the amine, it is first converted to a quaternary ammonium salt by methylation. Subsequent elimination is very rapid. The last example is an unconventional case in which an intramolecular Mannich precursor is generated in situ by an azaCope rearrangement.
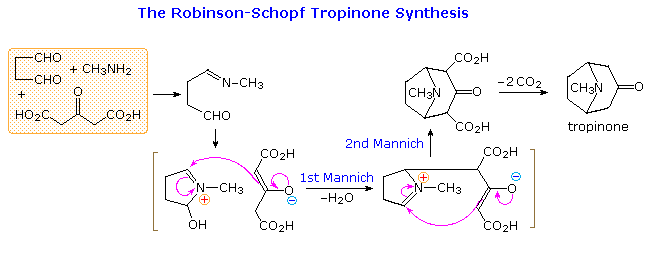
By clicking on the diagram a second time, a remarkable synthesis of the bicyclic aminoketone tropinone will appear above. This double Mannich sequence is known as the Robinson-Schopf synthesis in honor of the two chemists who first reported it in the first quarter of the 20th century. The reaction takes place in water under physiological conditions (pH and temperature), and in high yield.
 الاكثر قراءة في مواضيع عامة في الكيمياء العضوية
الاكثر قراءة في مواضيع عامة في الكيمياء العضوية
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة
قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)


















