

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء التناسقية

الكيمياء الاشعاعية والنووية
مقياس الجهد ( Potentiometer) ومقياس درجة الحموضة (pH-meter)
المؤلف:
د.عبدالله محمود ابو الكباش
المصدر:
الكيمياء التحليلية المفاهيم الاساسية في التحليل التقليدي والالي
الجزء والصفحة:
ص 160-161
2024-02-10
1528
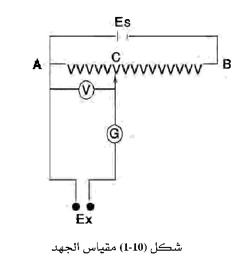
يستخدم مقياس الجهد للقياس في دوائر كهربائية منخفضة المقاومة، في حين يستخدم مقياس pH لقياس الجهد في حالة ما تكون المقاومة عالية جداً كما هي في القطب الزجاجي المستخدم لقياس .p . لقياس جهد في خلية ما يتم وصل هذه الخلية بجلفانوميتر ويوصل هذا الجلفانوميتر بخلية قياسية (ES) معروفة الجهد (Standard cell). وتتصل الخلية القياسية بالمقاومة AB وباستخدام موصل متحرك C يمكن التحكم في جهد الخلية. وعند قياس جهد خلية العينة Ex يتم تغيير وضع الموصل المتحرك C حتى يصبح جهد الخلية القياسية مساوياً لجهد خلية العينة Ex. وهذا يظهر عندما لا يكون هناك أي تيار في الجلفانوميتر. وعلى هذا الأساس يمكن قراءة جهد خلية العينة من الجلفانوميتر. وتمثل هذه القيمة الفرق بين جهد القطب الدليل والقطب المرجع في خلية العينة وحيث إن جهد قطب المرجع ثابت فإن التغيير في جهد القطب الدليل يدل على التغير في تركيز الأيون المراد تحليلية، وذلك حسب معادلة نيرنست (Nernst equation) وهذا هو المبدأ الذي تقوم عليه الطرق الجهدية.
 الاكثر قراءة في مواضيع عامة في الكيمياء التحليلية
الاكثر قراءة في مواضيع عامة في الكيمياء التحليلية
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة
قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)


















