


 علم الكيمياء
علم الكيمياء 
 الكيمياء التحليلية
الكيمياء التحليلية 
 الكيمياء الحياتية
الكيمياء الحياتية 
 الكيمياء العضوية
الكيمياء العضوية 
 الكيمياء الفيزيائية
الكيمياء الفيزيائية
 الكيمياء اللاعضوية
الكيمياء اللاعضوية 
 مواضيع اخرى في الكيمياء
مواضيع اخرى في الكيمياء
 الكيمياء الصناعية
الكيمياء الصناعية |
Read More
Date: 19-7-2016
Date: 26-7-2016
Date: 13-4-2017
|
Pure Water Is Slightly Ionized
Water molecules have a slight tendency to undergo reversible ionization to yield a hydrogen ion (a proton) and a hydroxide ion, giving the equilibrium
 (1.1)
(1.1)
Although we commonly show the dissociation product of water as Hˉ, free protons do not exist in solution; hydrogen ions formed in water are immediately hydrated to hydronium ions (H3O+). Hydrogen bonding between water molecules makes the hydration of dissociating protons virtually instantaneous:
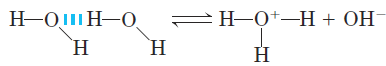
The ionization of water can be measured by its electrical conductivity; pure water carries electrical current as Hˉ migrates toward the cathode and OH+ toward the anode. The movement of hydronium and hydroxide ions in the electric field is anomalously fast compared with that of other ions such as Na+, K+, and Clˉ. This high ionic mobility results from the kind of “proton hopping” shown in Figure 1.1. No individual proton moves very far through the bulk solution, but a series of proton hops between hydrogen-bonded water molecules causes the net movement of a proton over a long distance in a remarkably short time. As a result of the high ionic mobility of H+ (and of OHˉ, which also moves rapidly by proton hopping, but in the opposite direction), acid-base reactions in aqueous solutions are generally exceptionally fast. As noted above, proton hopping very likely also plays a role in biological proton-transfer reactions. Because reversible ionization is crucial to the role of water in cellular function, we must have a means of expressing the extent of ionization of water in quantitative terms.
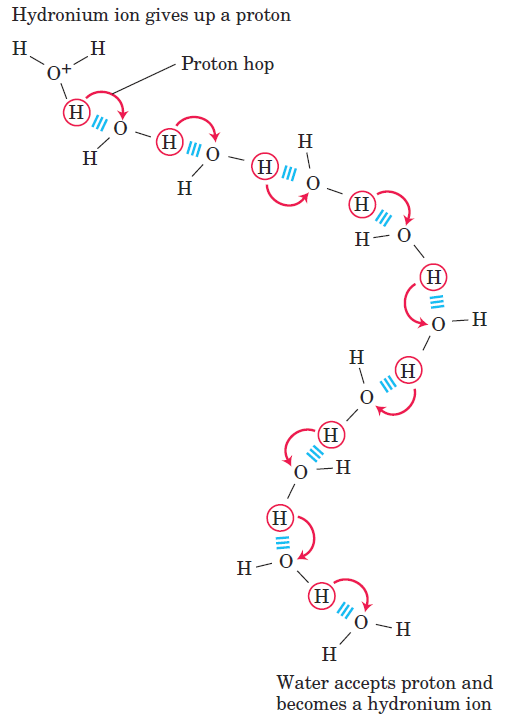
FIGURE 1.1 Proton hopping. Short “hops” of protons between a series of hydrogen-bonded water molecules effect an extremely rapid net movement of a proton over a long distance. As a hydronium ion (upper left) gives up a proton, a water molecule some distance away (lower right) acquires one, becoming a hydronium ion. Proton hopping is much faster than true diffusion and explains the remarkably high ionic mobility of H+ ions compared with other monovalent cations such as Na+ or K+.
A brief review of some properties of reversible chemical reactions shows how this can be done. The position of equilibrium of any chemical reaction is given by its equilibrium constant, Keq (sometimes expressed simply as K). For the generalized reaction
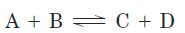 (1.2)
(1.2)
an equilibrium constant can be defined in terms of the concentrations of reactants (A and B) and products (C and D) at equilibrium:
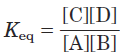
Strictly speaking, the concentration terms should be the activities, or effective concentrations in nonideal solutions, of each species. Except in very accurate work, however, the equilibrium constant may be approximated by measuring the concentrations at equilibrium. For reasons beyond the scope of this discussion, equilibrium constants are dimensionless. Nonetheless, we have generally retained the concentration units (M) in the equilibrium expressions used in this book to remind you that molarity is the unit of concentration used in calculating Keq. The equilibrium constant is fixed and characteristic for any given chemical reaction at a specified temperature. It defines the composition of the final equilibrium mixture, regardless of the starting amounts of reactants and products. Conversely, we can calculate the equilibrium constant for a given reaction at a given temperature if the equilibrium concentrations of all its reactants and products are known.



|
|
|
|
صنع الذكريات والتفكير يدمر الدماغ.. دراسة تشرح السبب
|
|
|
|
|
|
|
الصين.. عودة كاسحتي الجليد إلى شنغهاي بعد انتهاء بعثة استكشافية إلى القطب الجنوبي
|
|
|
|
|
|
جامعة الكفيل تكرم الفائزين بأبحاث طلبة كلية الصيدلة وطب الأسنان
|
|
|
|
مشروع التكليف الشرعي بنسخته السادسة الورود الفاطمية... أضخم حفل لفتيات كربلاء
|
|
|
|
ضمن جناح جمعيّة العميد العلميّة والفكريّة المجمع العلمي يعرض إصداراته في معرض تونس الدولي للكتاب
|
|
|
|
جامعة الكفيل تعقد مؤتمرها الطلابي العلمي الرابع
|