
 الجغرافية الطبيعية
الجغرافية الطبيعية 
 الجغرافية الحيوية
الجغرافية الحيوية 
 جغرافية التضاريس
جغرافية التضاريس 
 الجغرافية البشرية
الجغرافية البشرية 
 الجغرافية الاجتماعية
الجغرافية الاجتماعية 
 الجغرافية الاقتصادية
الجغرافية الاقتصادية 
 الاتجاهات الحديثة في الجغرافية
الاتجاهات الحديثة في الجغرافية |
أقرأ أيضاً
التاريخ: 22-12-2015
التاريخ: 23-12-2015
التاريخ: 30-11-2020
التاريخ: 23-12-2015
|
يطلق على الأراضي المتملحة تبعا لأغلب المراجع الحديثة اسم الأراضي المتأثرة بالأملاح وأبرز صفات هذه الأراضي ارتفاع تركيز الأملاح بها , وتنتشر هذه الأراضي في أغلب قارات العالم وتعتبر ملوحة الأرض من أهم العوامل المحددة للإنتاج الزراعي العالمي.
ولدراسة إصلاح الأراضى المتأثرة بالأملاح يلزم التعرف على ملوحة التربة ثم تصنيف الأراضى المتأثرة بالأملاح ثم العلاقة بين استخدام مياه الري وملوحة التربة ، وبعدئذ يلزم التعرف على كيفية الإصلاح ثم إمكانية التعايش مع ملوحة التربة.
1- ملوحة التربة Soil Salinity :
ملحية التربة أو ملوحتها ترجع إلى ارتفاع تركيز أنواع معينة من الأملاح في النظام الأرضي وتؤدى مصادر معينة إلى تراكم وتجمع هذه الأملاح بالتربة كما تكون بعض الظروف مشجعة ومناسبة لذلك التجمع . ويقوم الماء الأرضي بدور هام في ديناميكية وحركة الأملاح وتجمعها في التربة. وكنتيجة لوجود الأملاح تحدث في التربة بعض العمليات التكوينية Forming Processes كما تتأثر بعض خواص التربة (وبصفة خاصة ميزانها الملحي) نتيجة هذه الملوحة. وسنحاول فيما يلي توضيح كل من هذه النقاط على حدة .
2-الأملاح الشائعة في النظام الأرضي: تقسم الأملاح الشائعة في التربة تبعا لدرجة ذوبانها وعلاقتها بملوحة التربة إلى قسمين :
1- أملاح سريعة الذوبانReadily soluble salts مثل كلوريد الصوديوم( NaCl ) ، كلوريد المغنيسيوم ( MgCl2 ) ، كلوريد الكالسيوم(CaCl2) ، كبريتات الصوديوم ( Na2SO4 ) ، كبريتات المغنيسيوم ( MgSO4 ) ،كربونات الصوديوم ( Na2CO3 ) وهى المسئولة في الطبيعة عن ملوحة وقلوية التربة .
2-أملاح شحيحة الذوبان أو عديمة الذوبان: مثل كبريتات الكالسيوم ( CaSO4 )، كربونات المغنيسيوم ( MgCO3 ) ، كربونات الكالسيوم ( CaCO3 )، ويكون تأثيرها بدرجة اكبر على الخواص الطبيعية للتربة لقلة ذوبانها. وفيما يلي توضيح لكل من هذه الأملاح على حدة مع بيان علاقتها بملوحة التربة.
أ- أملاح الكربونات Carbonates :
تنتشر أملاح حامض الكربونيك Carbonic acid في الأراضي القاحلة وشبه القاحلة وسلوك وتأثير هذه الأملاح يعتمد على نوع الملح وتركيزه ودرجة ذوبانه ومدي سميته للنبات.
ومن أملاح حامض الكربونيك الشائعة في الأراضي ما يلي :
1- كربونات الكالسيوم Calcium carbonate (CaCO3 ): وهو ملح قليل الذوبان جدا في الماء ( 0.0131 جم/لتر ) وتزداد درجة ذوبانه إلى 0.14 جم / لتر في وجود حامض الكربونيك لتكوين بيكربونات الكالسيوم ( CA(HCO3) ) .وعندما يتحلل هذا الملح ينتج عنه تأثير قاعدي ( قاعدة قوية وحامض ضعيف ) ويكون رقم pH بين 0ر10 - 10.2 أما فى وجود حامض الكربونيك او غاز ثاني أكسيد الكربون فيكون رقم pH بين 7.9 - 8.5 . ونظرا لقلة ذوبان كربونات الكالسيوم فان وجوده في التربة لا يؤثر على معظم المحاصيل الزراعية ، إلا أن بعض المحاصيل تتأثر من حيث كمية المحصول وجودته في حالة وجود نسبة عالية من كربونات الكالسيوم في التربة مثل : أشجار الكاكاو – البن – الموز- الحمضيات .
وتحتوى غالبية مياه الأنهار والمياه الجوفية على نسبة لا باس بها من بيكربونات الكالسيوم الذائبة ومعظم الترسيبات المحمولة بواسطة مياه الأنهار والبحيرات تحتوى على نسبة عالية من كربونات الكالسيوم (7 – 15 % ) . وتترسب في آفاق قطاع التربة نتيجة تبخر المياه الجوفية القريبة من السطح كميات كبيرة من كربونات الكالسيوم.
وأحيانا تتجمع كربونات الكالسيوم في آفاق معينة من قطاع التربة ( قد تصل نسبتها فى التربة إلى 80 % ) وتتكون طبقة صلبة ذات نفاذية قليلة أو عديمة النفاذية مما يتسبب فى إعاقة حركة المياه وتغلغل الجذور في التربة . وتعمل كربونات الكالسيوم كمادة لاحمة ولها تأثير هام فى تكوين يناء التربة. ومن الممكن إن تقوم بدورها كمادة لاحمة في التربة بعد فترة ري ما بين 5-7 سنوات من تاريخ ترسيبها . ويمكن ملاحظة كربونات الكالسيوم فى التربة إذ يكون لها لون ابيض إما على شكل تجمعات أو على شكل عروق تشبه الميسيليوم الخاص بالفطر كما يمكن تقديرها في المعمل بطريقة كمية Quantitative .
2- كربونات المغنيسيوم Magnesium carbonate ( MgCO3 ): درجة ذوبانها أكثر من كربونات الكالسيوم وتزداد درجة الذوبان في وجود حامض الكربونيك أو غاز ثاني أكسيد الكربون . ولها تأثير ضار جدا على النباتات لأنه ينتج عن تحلل كربونات المغنيسيوم تأثير قاعدي وقد يصل رقم pH الي 0ر10 . ويعتبر وجود كربونات المغنيسيوم في الطبيعة بصورة حرة نادرا نظرا لتكوين معدن الدلوميت Dolomite وادمصاص المغنيسيوم على معادن الطين
3- كربونات الصوديومSodium carbonate ( Na2CO3 ) : أملاح حامض الكربونيك مع الصوديوم شائعة في الطبيعة وتتجمع في التربة في مناطق كثيرة وبكميات لا بأس بها.
وتتكون كربونات الصوديوم من التفاعل بين حامض الكربونيك وأيدروكسيد الصوديوم وتتبلور كربونات الصوديوم مع كميات مختلفة من الماء مكونة بلورات من Na2CO3.H2O أو Na2CO3.10H2O. كربونات الصوديوم ملح شديد الذوبان في الماء (178 جم/لتر) وتحلله المائي ينتج عنه وسطا قاعديا يصل رقم pH فيه إلي 12 ونظرا لشدة ذوبانه وتأثيره القاعدي القوى فإنه يكون شديد السمية لمعظم النباتات .ويؤدى وجود كربونات الصوديوم في التربة الي انتشار وتفريق Dispersion جزيئات الطين وهدم Destruction مجاميع البناء وما يصاحب ذلك من قلة النفاذية ونقص خصوبة التربة وإنتاجيتها حتى لو وجدت كربونات الصوديوم بتركيزات قليلة مثل 0.5 – 0.1 % .
وتعتبر بيكربونات الصوديوم اقل قاعدية من كربونات الصوديوم لأنها تنتج من التعادل الجزئي لكربونات الصوديوم مع حامض الكربونيك :
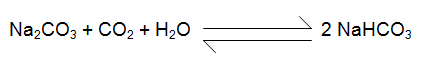
ويتجه التفاعل نحو تكوين البيكربونات في حالة التحلل الشديدة للمواد العضوية أو عندما تنخفض درجة الحرارة .وعلى العكس يتجه التفاعل لتكوين الكربونات إذا كان مفعول الأحياء الدقيقة على تحلل المادة العضوية ضعيف أو عندما ترتفع درجة الحرارة .
وعندما تتبخر المياه الجوفية المحتوية على هذين الملحين فانهما يترسبان في التربة بشكل ثنائي Na2CO3. NaHCO3. 2H2O أو على شكلNaHCO3 نقى . ونادرا ما توجد كربونات الصوديوم في الأراضي القاحلة أو الصحارى التي تحتوى نسبة عالية من الجبس نظرا لتحول كربونات الصوديوم إلى كربونات كالسيوم :
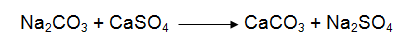
وتنخفض درجة ذوبان كربونات الصوديوم بشدة عندما تنخفض درجة الحرارة إلي أقل من 8 م وبذلك يصعب غسلها في فصل الشتاء .والأراضي التي تحتوى على هذين الملحين معا تكون ملحية قلوية لوجود ملحى كربونات وكبريتات الصوديوم معا وتحتاج معاملات خاصة أثناء الإصلاح.
4- كربونات البوتاسيوم : Potassium carbonate ( K2CO3 ): يعتبر وجودها في التربة أكثر ندرة من وجود كربونات الصوديوم ، ونظرا لشدة ذوبانه وقاعديته فانه يعتبر شديد السمية للنبات ويؤثر تأثير سيئا على خواص التربة الطبيعية وعمليا فان هذا الملح مشابه في تأثيره لملح كربونات الصوديوم.
(ب) أملاح الكبريتات Sulphates:
توجد أملاح حامض الكبريتيك في معظم الأراضي والمياه الجوفية بكميات مختلفة وتترسب هذه الأملاح في التربة بكميات لا باس بها. ويختلف تأثيرها على المحاصيل وعمليات الاستصلاح تبعا لاختلاف تركيب هذه الأملاح ومن أملاح الكبريتات الشائعة في الأراضي:
1- كبريتات الكالسيوم Calcium sulphate ( CaSO4 ): يعتبر ملح كبريتات الكالسيوم من الناحية الفسيولوجية عديم الضرر للنباتات لقلة ذوبانه في الماء ( 1.9 جم/لتر ) .
وتحتوي أراضي المناطق شبه الصحراوية على نسبة من الجبس تجمعت نتيجة تبخر المياه
المالحة بحيث أصبحت تربتها تحتوى على الجبس الذى تجمع منذ قديم الزمان .
وفى الصحاري حيث يكون الجو شديد الجفاف يتحول الجبس من CaSO4.2H2O إلى CaSO4.H2O أي يفقد جزئ من ماء التبلور .
ويوجد الجبس في التربة في أشكال مختلفة في صورة بلورات شفافة أو نصف شفافة أو صفائح منتظمة الشكل. وفى الأرضي التي تحتوى نسبة عالية من الجبس فان هذا الجبس يكون طبقة إسفنجية ذات كتلة مسامية تجعل طبقة القطاع متماسكة جدا. وهذه الطبقة تكون نفاذيتها للماء والهواء قليلة وتحدد تغلغل الجذور في التربة .
يستعمل الجبس كمادة مصلحة في استصلاح الأراضي القلوية التي تحتوى على نسبة عالية من أيون الصوديوم المتبادل .
2- كبريتات المغنيسيومMagnesium sulphate ( MgSO4 ) : ويوجد في صورة MgSO4. 7H2O وهو أحد الأملاح الرئيسية في الأراضي الملحية والمياه الجوفية المالحة ومياه البحيرات وبعض أنواع الطين. وذوبان كبريتات المغنيسيوم فى الماء عالي (262 جم/لتر) ولذلك يعتبر من الأملاح السامة والمؤذية للنباتات .
ولا تتجمع كبريتات المغنيسيوم مطلقا بصورة نقية في التربة بل تكون دائما مترسبة مع بعض الأملاح الأخرى .
3- كبريتات الصوديوم Sodium sulphate ( Na2SO4 ) : تعتبر أحد الأملاح الرئيسية في الأراضي المتأثرة بالأملاح والمياه الجوفية المالحة وفى مياه البحيرات وسمية هذا الملح أقل مرتين أو ثلاثة من ملح كبريتات المغنسيوم . درجة ذوبان كبريتات الصوديوم تعتمد على درجة حرارة الوسط إذ تزداد بزيادة درجة الحرارة ولذلك يكون وضع كبريتات الصوديوم في التربة معقدا إلى درجة كبيرة ففي المواسم الدافئة فان كبريتات الصوديوم ترتفع الي سطح التربة مع الأملاح الأخرى (كبريتات المغنيسيوم ، كلوريد المغنيسيوم ، كلوريد الصوديوم) وفى المواسم الباردة تغسل الأملاح الأخرى من سطح التربة ( نتيجة سقوط الأمطار) ويتبقى قسم من كبريتات الصوديوم في السطح حتى موسم ارتفاع درجة الحرارة . وعندما ترتفع درجة الحرارة يتحول معدن Mirabilite وتركيبه Na2SO4.10H2O والذي يوجد غالبا في صورة بلورات كبيرة شفافة الي معدن Thenardite ( Na2SO4 ) وهو عبارة عن مسحوق أبيض .
وأحيانا تتبلور كبريتات الصوديوم مع كبريتات الكالسيوم (الجبس) مكونة ما يسمى Glauberite (CaSO4. Na2SO) ، والأرض الملحية التي تحتوى على نسبة عالية من ملح كبريتات الصوديوم تحتاج الي كميات كبيرة من المياه لإزالة الأملاح بالغسيل ويفضل أن تجرى عملية الغسيل عندما تكون درجة الحرارة مرتفعة قليلا (دافئة) مع زراعة الأرز إذا كان ذلك ممكنا .
4- كبريتات البوتاسيوم Potassium sulphate ( K2SO4 ):لا تتجمع كبريتات البوتاسيوم في التربة بكميات كبيرة وخواصها تقريبا مشابهة لكبريتات الصوديوم ولكن سميتها أقل . وتوجد أحيانا بعض التكوينات الملحية التي تحتوى على نسبة عالية من كبريتات البوتاسيوم وهذه تستعمل كسماد .
(جـ ) الكلوريداتChlorides :
تكون الكلوريدات مع الكبريتات معظم الأملاح الرئيسية فى الأراضي المتملحة . وتتميز الكلوريدات بدرجة ذوبانها العالية في الماء وعليه فأنها جميعا تكون سامة للنبات. وبشكل عام كلما زادت نسبة الأملاح في التربة أو المياه الجوفية تزيد الكلوريدات (علاقة طردية) ومن الكلوريدات الشائعة في النظام الأرضي :
1- كلوريد الكالسيوم Calcium chloride (CaCl2 ) :يندر وجود كلوريد الكالسيوم في التربة حيث يتفاعل مع كبريتات الصوديوم وكربونات الصوديوم مكونا كربونات الكالسيوم أو كبريتات الكالسيوم التي تترسب في التربة . وعليه فإن كلوريد الكالسيوم يوجد في التربة أو محلولها أو في مياه البحيرات فقط عندما تكون درجة الملوحة عالية جدا ( 400 - 500 جم/لتر ) .و كلوريد الكالسيوم قد يوجد في الطبقة السطحية للأراضي شبه السولنشاك Solonchak like كنتيجة لتفاعل الإحلال التالي :
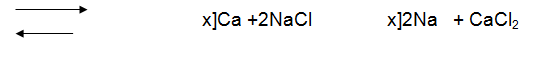
وتوجد كميات لا بأس بها من أملاح كلوريد الكالسيوم في المياه الجوفية العميقة مرتبطة مع بغض الترسيبات البترولية وقد ترتفع هذه المياه إلى السطح عن طريق الشقوق .
ويعتبر كلوريد الكالسيوم ملح سام ولكنه اقل سمية من كلوريد المغنيسيوم أو الصوديوم .
2- كلوريد المغنيسيوم Magnesium chloride ( Mg Cl2 ) :وهو أحد الأملاح الشائعة في الأراضي والمياه الجوفية المالحة ويتجمع هذا الملح بكميات كبيرة في حالة الأراضي الشديدة الملوحة . وهو ملح سام جدا للنبات نظرا لدرجة ذوبانه العالية ( 353 جم/لتر ) وقد يوجد بكميات كبيرة في المياه الجوفية العميقة . وقد يصعد كلوريد المغنيسيوم عن طريق الشقوق او عن طريق التفاعل التبادلي بين الصوديوم المذاب والمغنيسيوم المتبادل على سطح الطين ( مثلما يحدث مع كلوريد الكالسيوم ) .
ويعتبر كلوريد المغنيسيوم و كلوريد الكالسيوم ملحان متميعان يمتصان الرطوبة من الجو وخاصة عندما تكون درجة حرارة الجو منخفضة . ولذلك فان مظهر التربة الملحية التي تحتوى هذين الملحين يكون مبتلا دائما خاصة بعد سقوط الأمطار أو الندى . والأراضي الملحية التي تحتوى كمية كبيرة من كلوريد المغنيسيوم تحتاج إلى غسيل مركز للتخلص منه.
3- كلوريد الصوديوم Sodium chloride ( NaCl ):يعتبر كلوريد الصوديوم مع كلوريد و كبريتات المغنيسيوم من المكونات الرئيسية الشائعة للتربة الملحية. ودرجة سمية كلوريد الصوديوم عالية نظرا لارتفاع درجة ذوبانه في الماء
( 264 جم/لتر ) و حتى لو وجد بتركيزات منخفضة فان النباتات سوف تتأثر سلبيا .
والأرض المالحة التي تحتوى على 2- 5 % كلوريد الصوديوم نراها جرداء وعمليا فإن إستصلاح مثل هذه الأرض لا يكون الا بالغسيل لإزالة الأملاح التي توجد فيها.
وتسهل عملية غسيل كلوريد الصوديوم إذا كانت الأرض تحتوى على الجبس .
وفى معظم المناطق القاحلة وشبه القاحلة يمتص الصوديوم على معقد الادمصاص فى التربة أثناء عملية الغسيل ويسبب إنتشار جزيئات الطين وقلة النفاذية وإعاقة عملية الإصلاح .
4- كلوريد البوتاسيوم ( Potassium chloride ( KCl:كلوريد البوتاسيوم يشبه كلوريد الصوديوم من حيث التركيب الكيميائي ولو أن كلوريد البوتاسيوم لا يوجد بكثرة في التربة مثل كلوريد الصوديوم نظرا لاستهلاك الأحياء الدقيقة للبوتاسيوم بالإضافة إلى انه يكون عرضة للادمصاص العكسي على حبيبات الطين .
وإذا وجد كلوريد البوتاسيوم بنسبة عالية فان سميته للنبات تكون مشابهة لسمية كلوريد الصوديوم . وعموما فانه في الأراضي شديدة الملوحة يكون كلوريد البوتاسيوم قليل الوجود فيها. ونظرا لأهمية البوتاسيوم كعنصر غذائي فان ترسيبات هذا الملح تعتبر ذات أهمية في التسميد. ويوصى باستعمال أسمدة كلوريد البوتاسيوم أو على شكل Granallite
(MgCl2. KCl. 6H2O) في الأراضي الغير مالحة ولكن لا يوصى باستعمالها في الأراضي الملحية .
( د ) النترات Nitrates :
أملاح حامض النتريكHNO3 تعتبر أملاحا في غاية الأهمية كسماد آزوتي للتربة . وهذه الأملاح لا تتجمع بكميات كبيرة في التربة ( لا تتجاوز 0.05 % ) وفى بعض الحالات الاستثنائية في المناطق الصحراوية في شيلي والهند تتسبب نترات الصوديوم والبوتاسيوم بالإضافة الي كلوريد الصوديوم والبوتاسيوم في ملوحة التربة وتصبح التربة جرداء وفى هذه المناطق تصل نسبة النترات الى 50 % .
وبصفة عامة إذا زادت نسبة النترات في الأرض عن 0.07 – 0.1 % تصبح ضارة بالنباتات ويكون ضررها أكثر من ضرر الكلوريدات ويمكن التخلص من النترات بسهولة أثناء عملية الغسيل لشدة ذوبانها .وفى الظروف اللاهوائية Anaerobic conditions في المستنقعات أو عند زيادة الري عن اللازم تقل نسبة الأكسجين وعندئذ تختزل النترات بواسطة الأحياء الدقيقة إلي أمونيا NH3 أو غاز النيتروجين N2 .
( هـ ) البورات Borates:
من النادر وجود أملاح حامض البوريك H3BO3 في التربة ولو أنه يوجد في منطقة
البراكين بأمريكا اللاتينية وبعض المناطق الساحلية بحوض البحر المتوسط في أفريقيا والساحل الشمالي في مصر .
(و) مصادر الأملاح في الأرض : يقسم العالم الروسي Kovda مصادر الأملاح كما يلي :
1- مصادر قارية Continental :تتكون أملاح أحماض الكربونيك والكبريتيك والهيدروكلوريك في المناطق الداخلية التي لا يحدث فيها جرف الأرض بواسطة الماء الجاري Run-off نتيجة عمليات تجوية الصخور النارية Igneous Rocks (كما في أراضي منغوليا ومنشوريا) أو من الصخور الثانوية Secondary Rocks الغنية بالأملاح (كما في أراضي سيكيانج وإيران).
2- مصادر بحرية Marine :تنتج عن تجمع أملاح البحر وبصفة خاصة كلوريد الصوديوم في الوديان الساحلية للأراضي الجافة وعلى سواحل الخلجان الضحلة – ويصل تركيز الأملاح في بعض المواقع الي 150 جم/لتر وكثيرا ما يزيد كلوريد المغنيسيوم فيها عن كلوريد الصوديوم .
3- مصادر الدلتا Delta :وهى واسعة الانتشار وذات أهمية كبيرة لأن الإنسان تمكن من ري دلتا الأنهار من أقدم العصور. وتتميز دلتا الأنهار بالازدواج بين عمليات نقل الأملاح من القارة بواسطة الأنهار وعمليات تراكم الأملاح المنقولة من البحر في أوقات مختلفة.
4- مصادر جوفية Artisan:ويحدث ذلك بتبخير المياه الجوفية العميقة ثم تجمع الأملاح في المنخفضات القارية مثل منخفض القطارة في مصر.
5- مصادر بشرية Anthropogenic : وهى المتصلة بأخطاء النشاط الاقتصادي للإنسان وعدم معرفة القواعد التي تحكم تجمع الأملاح مثل تملح الأراضي المروية الناتج عن ارتفاع مستوي الماء الأرضي والري بالمياه المالحة .
رأى فالتر(Walter, 1961 ) : يرى فالترأن الأملاح يمكن أن تتكون من :
أ – من بخر مساحات كبيرة من المياه مثل بحر قزوين Caspian Sea والبحيرة المالحة الكبرى Great salt lake في ولاية يوتاه بالولايات المتحدة الأمريكية .
ب- من الصخور الرسوبية البحرية التي ساهمت الأملاح في عملية ترسيبها في البحر وعندما تنحسر عنها المياه وتتعرض للتجوية تظهر الأملاح على السطح.
ج- من الترسيب بالرياح Aeolic Sedimentation حيث ترسب الأتربة المحملة بالأملاح أو رذاذ البحر بعد نقلها من مواقعها بواسطة الرياح.
رأى كيلي(Kelly, 1950) :يرى كيلي أن تجوية الصخور النارية تعتبر بطريقة مباشرة أو غير مباشرة مصدرا هاما من مصادر الكلور ور كما أن الغازات المتصاعدة من البراكين وهى عادة غنية في كلورور الإيدروجين (في صورة غاز) قد ساهمت مساهمة هامة في وجود الكلوريدات في الأراضي والبحار ، وكذلك الحال بالنسبة للكبريتات إذ توجد نواتج أكسيد الكبريت في غازات البراكين بكميات وفيرة فضلا عن أن أكسدة الكبريتورات ومنها كبريتور الحديد ( البيريت) تعطى كبريتات .ومن أراء كل من كوفدا وفالتر وكيلي يتضح أن الأملاح قد تكونت في الأرض نتيجة لعمليات تجوية بعض معادن المادة الأرضية Soil material أو أنها انتقلت إليها من مواقع غنية بها خصوصا البحار بواسطة الرياح أو الأنهار ويرجع أغلب الباحثين أن الأراضي التي توجد بها الأملاح نتيجة النقل أكثر شيوعا من الأراضي التي تكونت فيها الأملاح بتجوية معادنها .
(ف) الظروف المناسبة لتجمع الأملاح في التربة : تتجمع الأملاح في الارض عندما تتوفر ظروف معينة :
أ- من الناحية الجيومورفولوجيةGeomor phology : تتجمع الأملاح عادة في المواقع المنخفضة مثل وديان الأنهار ودلتاها وشواطئ البحار والمحيطات .
(ب) من الناحية الهيدروجيولوجية Hydrogeology : تتجمع الأملاح في المساحات ذات القوام الطيني الثقيل نسبيا ومستوى الماء الأرضي المرتفع بحيث يستطيع هذا الماء أن يصل الي السطح بالخاصة الشعرية .
(ج) من الناحية الهيدرولوجية Hydrology :تتجمع الأملاح في المناطق التي لا يحدث فيها جرف للأرض بواسطة المياه الجارية وحيث يحكم البخر و النتح ميزان الماء الأرضي .
(د) من الناحية المناخية Climate : تتجمع الأملاح فى المناطق الجافة التي يزيد فيها البخر على المطر.
ويحكم تجمع الأملاح في الأراضي المروية ثلاث عوامل رئيسية وهى :
1- مقدار الماء الذي يضاف في كل رية .
2- عمق الماء الأرضي وتركيز الأملاح فيه .
3- مقدار المطر الساقط .
|
|
|
|
صنع الذكريات والتفكير يدمر الدماغ.. دراسة تشرح السبب
|
|
|
|
|
|
|
بركان ينفت الذهب في أقصى جنوب الأرض.. ما القصة؟
|
|
|
|
|
|
خلال الأسبوع الحالي ستعمل بشكل تجريبي.. هيئة الصحة والتعليم الطبي في العتبة الحسينية تحدد موعد افتتاح مؤسسة الثقلين لعلاج الأورام في البصرة
|
|
|
|
على مساحة (1200) م2.. نسبة الإنجاز في مشروع تسقيف المخيم الحسيني المشرف تصل إلى (98%)
|
|
|
|
تضمنت مجموعة من المحاور والبرامج العلمية الأكاديمية... جامعتا وارث الأنبياء(ع) وواسط توقعان اتفاقية علمية
|
|
|
|
بالفيديو: بعد أن وجه بالتكفل بعلاجه بعد معاناة لمدة (12) عاما.. ممثل المرجعية العليا يستقبل الشاب (حسن) ويوصي بالاستمرار معه حتى يقف على قدميه مجددا
|